TЯИАћвбОБЛЗЂЯж60грФъСЫЃЌШЛЖјШдгаКмЖрУеЭХС§ежзХTЯИАћЁЃ
ЁЁЁЁЮвУЧЖМжЊЕРЃЌЯИАћЖОадTЯИАћЪЧЭЈЙ§БэУцЕФTЯИАћЪмЬхЃЈTCRЃЉЪЖБ№ВЂЩБЫРАЉЯИАћЃЌЖјЧвTЯИАћЛЙЪЧИіСЌЛЗЩБЪжЃЌПЩвдСЌајЛїЩБЖрИіАЉЯИАћЁЃ
ЁЁЁЁШЛЖјЃЌдкЩЯЪіЛїЩБЙ§ГЬжаЃЌгаИіЮЪЬтРЇШХзХПЦбЇМвЃКTЯИАћОПОЙЪЧШчКЮднЭЃЩБЩЫаХКХВЂгыБЛжяЩБЕФАЉЯИАћЗжРыЃЌНјЖјЪЕЯжDouble killЁЂTriple killЁЁЃЌЩѕжСacedЕФЁЃ
ЁЁЁЁвЛжБвдРДЃЌПЦбЇМвЖМУЛгаИуЧхГўБГКѓЕФдвђЃЌжБЕНВЛОУЧАНЃЧХДѓбЇGillian M. GriffithsЭХЖгНЋИпЗжБцТЪЕчзгЯдЮЂОЕЖдзМСЫTЯИАћКЭАЉЯИАћЕФНгДЅЮЛЕуЁЊЁЊУтвпЭЛДЅ[1]ЁЃ
ЁЁЁЁGriffithsЭХЖгЛљгкШ§ЮЌжиНЈММЪѕзЗзйСЫTCRдкУтвпЭЛДЅаЮГЩЙ§ГЬжаЕФУќдЫЃЌВЂЗЂЯжTCRБЛМЄЛюжЎКѓЃЌЛсЕМжТУтвпЭЛДЅДІЕФTЯИАћФЄПьЫйЬиЛЏЃЌаЮГЩаЏДјзХЛюЛЏTCRЕФЭтФвХнЃЌЭбРыTЯИАћЃЌБЛАЉЯИАћЭЬЪЩЁЃЫцзХЭтФвХнЕФЭбТфВЂБЛАЉЯИАћЭЬЪЩЃЌЯИАћЖОадTЯИАћЕУвдгыАЉЯИАћЗжРыЃЌДгЖјЪЙTЯИАћОпБИСЌајЩБЩЫЕФФмСІЁЃ
ЁЁЁЁгЩгкдкДЫжЎЧАЃЌгаПЦбЇМвШЯЮЊTЯИАћБэУцTCRЕФМѕЩйЪЧвђЮЊФкЭЬКЭЫцКѓЕФНЕНтЕМжТЕФЃЛвђДЫЃЌПЩвдЫЕGriffithsЭХЖгЕФетвЛЗЂЯжгжЫЂаТСЫЮвУЧЖдTЯИАћЕФШЯжЊЁЃЯрЙибаОПГЩЙћЗЂБэдкЖЅМЖЦкПЏЁЖПЦбЇЁЗЩЯЁЃ
 ТлЮФЪзвГНиЭМ
ТлЮФЪзвГНиЭМЁЁЁЁСЌајЛїЩБАЉЯИАћЪЧЯИАћЖОадTЯИАћПЙАЉЕФЙиМќФмСІЁЃ
ЁЁЁЁетвЛЙ§ГЬПДЫЦМђЕЅЃЌЪЕМЪЩЯАЕВиаўЛњЁЃвђЮЊЃЌСЌЩБЩцМАЕНЪЖБ№ЁЂЛїЩБЁЂЗжРыЃЌдйЪЖБ№ЁЂдйЛїЩБЁЂдйЗжРыЕШвЛЯЕСабЛЗЕФИДдгЙ§ГЬЃЌУПвЛВНЖМашвЊTЯИАћЕФОЋзМПижЦЁЃ
ЁЁЁЁдкЯИАћЖОадTЯИАћЕФБэУцЃЌTCRЃЈАќРЈІССДКЭІТСДЃЉгыCD3ЃЈАќРЈІУЁЂІФЁЂІХКЭІЮЫФВПЗжЃЉзщГЩTCR-CD3ИДКЯЬхЃЌЙВЭЌИКд№ПЙдЕФЪЖБ№КЭаХКХЕФДЋЕнЁЃ
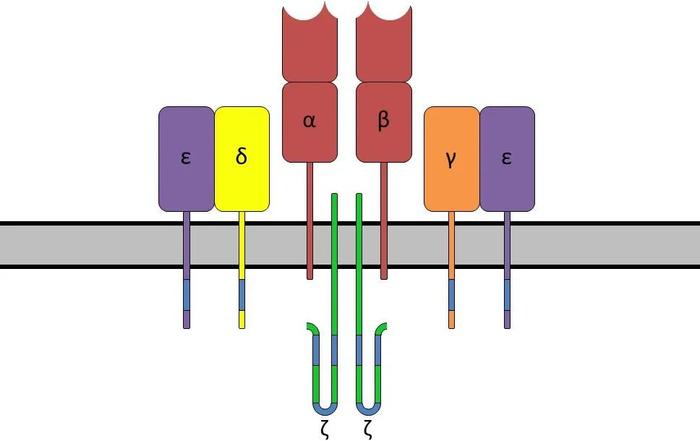 TCR-CD3ИДКЯЬхМАаХКХДЋЕн
TCR-CD3ИДКЯЬхМАаХКХДЋЕнЁЁЁЁGriffithsЭХЖгЪзЯШгУПЙЛЕбЊЫсЙ§бѕЛЏЮяУИЃЈAPEXЃЉБъМЧСЫCD3ІЮЃЌНЋБЛБъМЧЕФЯИАћЖОадTЯИАћгыАаЯИАћЃЈEL4ЃЌаЁЪѓСмАЭСіЯИАћЃЉЙВХрбјЃЌШЛКѓгУЕчзгЯдЮЂОЕЃЈEMЃЉНјааЖЯВуЩЈУшГЩЯёЁЃ
ЁЁЁЁДгЯТЭМВЛФбПДГіЃЌCD3ІЮ-APEXжївЊОлМЏдкTЯИАћЃЈЛвЩЋЃЉгыАЉЯИАћЃЈРЖЩЋЃЉНгДЅЕФВПЮЛЁЃ
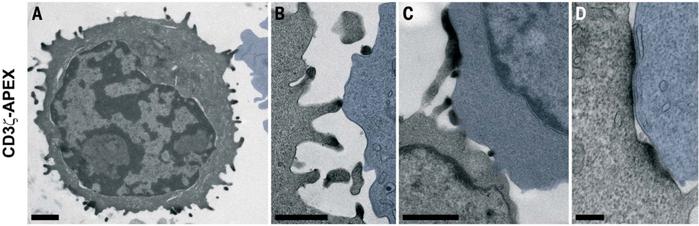 CD3ІЮ-APEXГЩЯёНсЙћ
CD3ІЮ-APEXГЩЯёНсЙћЁЁЁЁжиНЈЖЯВуЭМЕФНсЙћЯдЪОЃЌдкЯИАћЖОадTЯИАћгыАЉЯИАћЯрНгДЅЕФЮЛжУЃЌCD3ІЮ-APEXЃЈЯТЭМТЬЩЋЃЉдкЯИАћЖОадTЯИАћФЄЃЈЯТЭМбѓКьЩЋЃЉЩЯеМОнСЫвЛИіГЄДя2ІЬmЁЂПэДѓгк1ІЬmЕФЧјгђЃЌетИіЧјгђИеКУгыЯдЮЂОЕЙлВьЕНЕФTCRДиЯрЖдгІЁЃЪЕМЪЩЯЃЌЙлВьЕНЕФетИіАќКЌTCRЕФНсЙЙгаИіУћзжЃЌНаЁАжабыГЌЗжзгЛюЛЏДиЃЈcSMACsЃЉЁБ[2]ЁЃ
ЁЁЁЁЫфШЛДгГЩЯёНсЙћЩЯПЩвдПДЕНCD3ІЮ-APEXгыФ§МЏЫиАќБЛЕФФкЯнКЭНјШыЯИАћЖОадTЯИАћФкВПЕФаЁЙмгаЙиЃЌЕЋЪЧДѓЖрЪ§CD3ІЮ-APEXДцдкгкжБОЖЮЊ37жС210nmЕФЭтФвХнжаЃЌЖјЧветаЉЭтФвХнДгCD3ІЮ-APEXБъМЧЕФcSMACБпдЕЯђЭтУШЗЂЁЃЖЈСПЗжЮіНсЙћжЄЪЕЃЌАќКЌCD3ІЮЕФФвХн98%ЪЧЭтФвХнЃЌетвЛНсЙћжБЙлЕиБэУїЃЌУтвпЭЛДЅжаTCRЕФМѕЩйЪЧЭЈЙ§ЭтУкЖјЗЧФкЭЬЕїНкЕФЁЃ
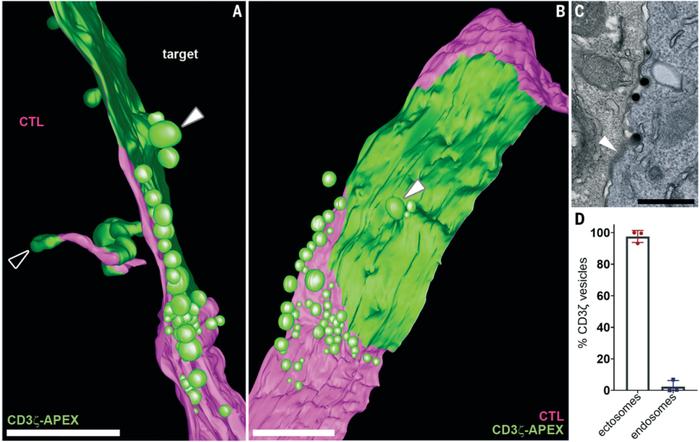 ПЩвдЗЧГЃУїЯдЕиПДГіЃЌаЏДјTCRЕФЭтФвХнБЛЪЭЗХ
ПЩвдЗЧГЃУїЯдЕиПДГіЃЌаЏДјTCRЕФЭтФвХнБЛЪЭЗХЁЁЁЁжЕЕУзЂвтЕФЪЧЃЌЖЈСПЗжЮіЛЙЗЂЯжЃЌЫцзХЪБМфЕФЭЦвЦЃЌАќКЌCD3ІЮЕФЭтФвХндіМгЃЌTЯИАћФЄЩЯЕФCD3ІЮМѕЩйСЫЃЌетБэУїTCRЧјгђУцЛ§ЕФМѕЩйЪЧЭтУкзїгУЕФНсЙћЁЃ
ЁЁЁЁШ§ЮЌЖЯВуЩЈУшКЭДЋЭГЕФЕчОЕЩЈУшвВЯдЪОЃЌдкЯИАћЖОадTЯИАћЗжУкЭтФвХнЕФЕиЗНЃЌTЯИАћКЭАЉЯИАћжЎМфЕФНгДЅБфЕУВЛНєУмСЫЃЌЩѕжСЪЧГіЯжСЫЧхЮњПЩМћЕФЗжРыЁЃ
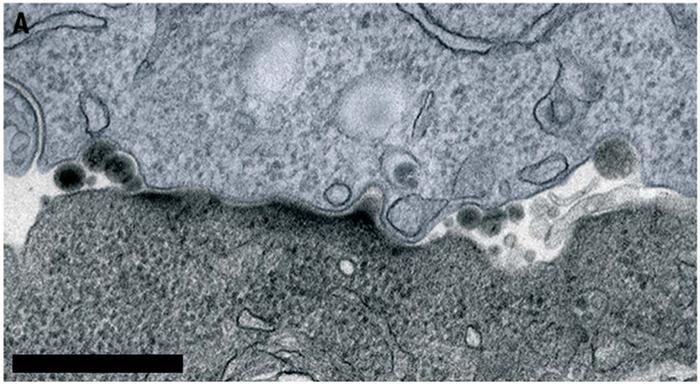 ЗжУкЭтФвХнЕФЕиЗНУїЯдЗЂЩњСЫЗжРы
ЗжУкЭтФвХнЕФЕиЗНУїЯдЗЂЩњСЫЗжРыЁЁЁЁGriffithsКЭЫћЕФЭЌЪТШЯЮЊЃЌвдЩЯбаОПНсЙћБэУїЃЌАќКЌTCRЕФЭтФвХнЕФЭбТфЃЌМШФмНЋTCRДгУтвпЭЛДЅжавЦГ§ЃЌгжФмЦєЖЏЯИАћЖОадTЯИАћгыАЉЯИАћжЎМфЕФЗжРыЁЃ
ЁЁЁЁдкЩЯЪіГЩЯёбаОПЕФЛљДЁЩЯЃЌGriffithsЭХЖгЛЙЗЂЯжЃЌЯИАћЖОадTЯИАћЗжУкЕФАќКЌTCRЕФЭтФвХнзюжеЪЕМЪЩЯЪЧНјШыСЫАаЯИАћЁЃЖјЧвЃЌЛюЛЏЕФTCRвЛЕЉЭбРыTЯИАћЃЌTЯИАћжаЕФМЄЛюаХКХДЋЕнвВОЭЫцжЎжежЙСЫЁЃ
ЁЁЁЁвВОЭЪЧЫЕЃЌTЯИАћЭЈЙ§ЭтУкЕФаЮЪНЪЭЗХTCRЃЌВЛНіФмАяжњTЯИАћАкЭбАаЯИАћЕФЪјИПЃЌШУЦфМЬајЩБЕаЃЛЛЙФмжежЙTЯИАћФкВПЕФМЄЛюаХКХЃЌЗРжЙЦфДІгкЙ§ЖШЛюЛЏЕФзДЬЌЁЃ
ЁЁЁЁжСгкАќКЌTCRЭтУкЬхЕФЗжУкЛњжЦЃЌGriffithsЭХЖгвВзіСЫЬНЬжЁЃдРДЃЌTCRЕФЛюЛЏЛсВњЩњИЪгЭЖўѕЅЃЈDAGЃЉЃЌетИіDAGДјРДЕФИКФЄЧњТЪЛсЦєЖЏDAGзщГЩЕФЭтФвХнНЋTCRЗжУкЕНTЯИАћЭтЁЃ
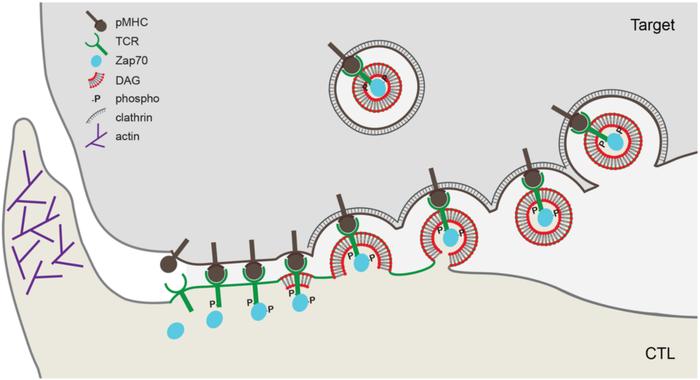 GriffithsЭХЖгЭЦВтЕФЭтФвХнЗжУкЛњжЦ
GriffithsЭХЖгЭЦВтЕФЭтФвХнЗжУкЛњжЦЁЁЁЁвЛжБвдРДЃЌКмЖрбаОПЗЂЯжTЯИАћЕФTCRдкБЛМЄЛюжЎКѓОЭЛсМѕЩйЃЌЫфШЛTCRЕФФкЭЬКЭЫцКѓЕФНЕНтвЛжББЛШЯЮЊЪЧTCRЯТЕїЕФЙиМќЛњжЦ[3]ЃЌЕЋGriffithsЭХЖгЕФбаОПБэУїЃЌдкУтвпЭЛДЅжаВЂЗЧШчДЫЃЌЛюЛЏЕФTCRЪЕМЪЩЯЪЧЭЈЙ§ЭтУкзїгУБЛХХГіСЫTЯИАћЁЃ
ЁЁЁЁзмЕФРДЫЕЃЌетИіОпгаЕпИВадЕФбаОПГЩЙћЗсИЛСЫЮвУЧЖдЯИАћЖОадTЯИАћзїгУЛњжЦЕФРэНтЁЃЭЈЙ§ЭтУкЛюЛЏЕФTCRЃЌЯИАћЖОадTЯИАћПЩвджежЙЯИАћаХКХДЋЕМЃЌВЂЭбРыЕБЧАФПБъЃЛШУЦфОпБИЩБЫРЯТвЛИіАаЯИАћЧвВЛЛсЩЫМАЮоЙМЕФФмСІЁЃдкетИібаОПЕФЛљДЁЩЯЃЌФПЧАЛљгкTЯИАћЕФПЙАЉСЦЗЈЃЌЛђаэПЩвдзіНјвЛВНЕФИФНјЩ§МЖЁЃ
ЁЁЁЁВЮПМЮФЯзЃК
ЁЁЁЁ[1].Stinchcombe JC, Asano Y, Kaufman CJG, et al. Ectocytosis renders T cell receptor signaling self-limiting at the immune synapse. Science. 2023;380ЃЈ6647ЃЉ:818-823. doi:10.1126/science.abp8933
ЁЁЁЁ[2].Monks CR, Freiberg BA, Kupfer H, Sciaky N, Kupfer A. Three-dimensional segregation of supramolecular activation clusters in T cells. Nature. 1998;395ЃЈ6697ЃЉ:82-86. doi:10.1038/25764
ЁЁЁЁ[3].Alcover A, AlarcЈЎn B, Di Bartolo V. Cell Biology of T Cell Receptor Expression and Regulation. Annu Rev Immunol. 2018;36:103-125. doi:10.1146/annurev-immunol-042617-053429

















