mRNA技术因为在新冠疫苗中的成功应用而受到广泛关注,对于预防性疫苗而言,mRNA通过表达来自病原体的蛋白来诱导免疫反应。此外,还有一些临床研究使用mRNA表达癌细胞的抗原来诱导免疫反应,用作癌症疫苗。除此之外,mRNA疗法还可以在体内生成蛋白质,从而替代罕见遗传病中的异常蛋白或缺失蛋白。
而一项最新临床试验表明,疫苗并非mRNA技术的唯一应用。
2024年4月3日,杜克大学医学院、多伦多大学病童医院、加州大学洛杉矶分校、伯明翰大学、伦敦大奥蒙德街儿童医院与Moderna公司的研究人员合作,在国际顶尖学术期刊 Nature 上发表了题为:Interim analyses of a first-in-human phase 1/2 mRNA trial for propionic acidaemia 的研究论文。
该论文报告了Moderna公司开发的mRNA疗法mRNA-3927在治疗罕见遗传病丙酸血症的首次人体临床试验的中期数据,展现了安全且有前景的治疗效果,将患者危及生命的代谢失代偿事件风险降低了70%。

这项鼓舞人心的临床试验结果推动了mRNA技术的应用,点燃了人们对mRNA技术期待已久的希望――直接在体内生成治疗性蛋白,作为蛋白替代疗法。
mRNA技术先驱、2023年诺贝尔生理学或医学奖得主 Katalin Kariko 表示,这项研究是朝着正确方向迈出的第一步。

丙酸血症(Propionic acidaemia,PA)是一种罕见的遗传疾病,由PCCA或PCCB基因的致病突变所致,这两个基因分别表达丙酰辅酶A羧化酶α亚基(PCCα)和β亚基(PCCβ),它们组成了丙酰辅酶A羧化酶(PCC),这是一种线粒体酶,在丙酸代谢途径中催化丙酰辅酶A向甲基丙二酰辅酶A的转化。而PCC的缺乏会导致有毒代谢物在血液和其他组织中积聚,并损害重要器官(包括心脏和大脑)。丙酸血症的出生患病率因地区而异,大约10万-15万人中有1人患病,通常在新生儿或婴儿时期发病。
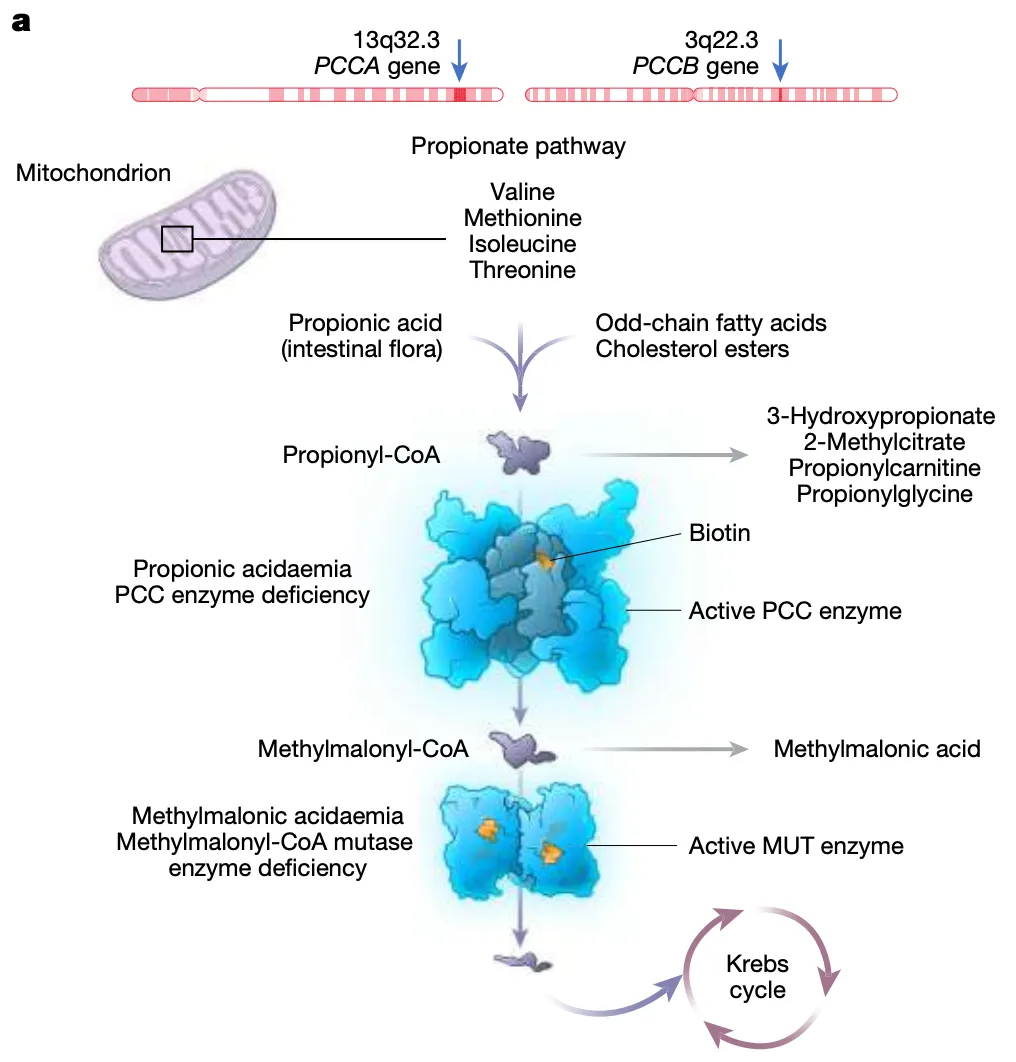
丙酸血症以危及生命的代谢失代偿事件(MDE)为特征,通常出现在新生儿中,表现为呕吐、脱水、体重减轻、喂食困难和总体临床状况的急性恶化。这种表现通常伴随着进行性脑病,表现为嗜睡、癫痫发作、觉醒减少和昏迷,如果不及时治疗,可能会导致残疾甚至死亡。丙酸血症的多系统并发症包括生长迟缓、神经系统表现、心肌病、心律失常、复发性胰腺炎、骨髓抑制和易感染性。
目前,可以通过特殊饮食等措施来控制丙酸血症患者的病情,但还没有能够直接从根本上解决病因的治疗方法,大多数患者仍然存在严重的健康问题。
早期干预对于预防丙酸血症患者的代谢失代偿、降低死亡率以及改善患者的预后至关重要。然而,目前还没有获批的药物可以直接解决患者发病的根本原因――丙酰辅酶A羧化酶(PCC)缺陷。
mRNA-3927是一款由Moderna公司开发的脂质纳米颗粒(LNP)递送的mRNA疗法,其由两个mRNA组成,一个编码正常的人PCCα亚基,另一个编码正常的人PCCβ亚基。静脉注射mRNA-3927后,能够靶向进入肝脏细胞,进而在肝脏中恢复功能性的PCC酶。
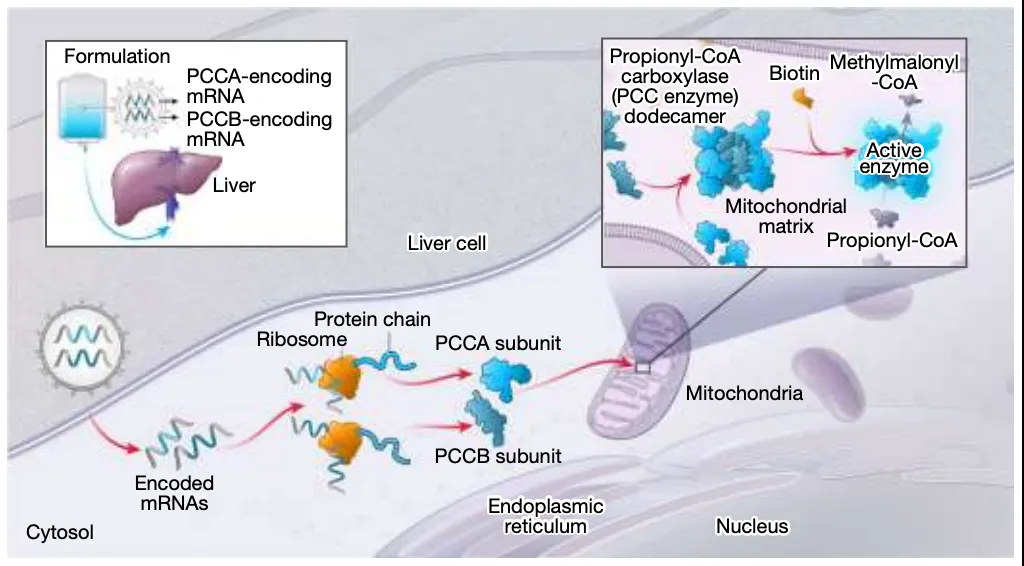
这项1/2期临床研究旨在评估mRNA-3927在1岁或以上丙酸血症患者中的安全性和有效性。截至2023年5月31日,共有5个剂量组的16名丙酸血症患者入组。16名患者中有12名完成了剂量优化研究并参加了扩展研究。患者在每两周到三周通过长达数小时的输注缓慢给药,输注剂量是mRNA新冠疫苗的数百倍。
16名丙酸血症患者中有8名在开始治疗前一年经历了危及生命的代谢失代偿事件,对于这8名患者,研究期间此类代谢失代偿事件的发生率降低了70%,此外,研究期间他们血液中的疾病相关代谢物水平也呈下降趋势,这提示了肝脏正在制造丙酰辅酶A羧化酶(PCC),但需要进行侵入式肝脏活检验证这一点。治疗相关的不良反应包括发热、呕吐和腹泻,但这些不良反应都不被认为是剂量限制性的。
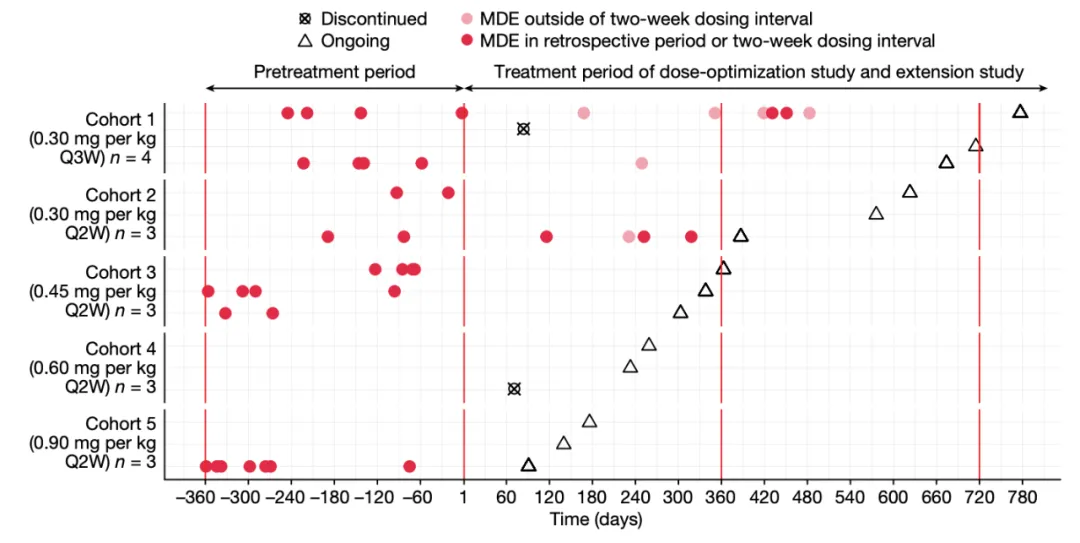
最后,论文作者指出,该临床研究由于样本量小和缺少对照组,无法通过统计学分析来评估研究结果的显著性。但这项研究仍在继续,中期分析的初步迹象表明该mRNA疗法对丙酸血症这种罕见遗传病具有潜在临床获益。
Moderna公司疗法开发主管 Kyle Holen 表示,公司目前正在招募更多临床试验参与者,以推动mRNA-3927朝着上市批准的目标前进。
长期以来,科学家们一直在担心mRNA疗法重复注射可能会引发针对治疗的免疫反应。而这项研究让我们确信,长期、重复注射大剂量的含有mRNA的LNP不会引起免疫反应,从而使mRNA疗法变得不安全或降低治疗获益,这对整个mRNA技术领域来说是一个非常重要的里程碑。
论文链接:
https://www.nature.com/articles/s41586-024-07266-7

















