引言:历史性的一刻
就在刚刚过去的1月30日,全球长寿科技圈迎来了一场地震级别的“官宣”。
美国食品药品监督管理局(FDA)正式为 Life Biosciences 开了绿灯,批准其启动一项极具科幻色彩的人体临床试验。这项试验将测试一种基于“部分表观遗传重编程”的基因疗法,旨在逆转细胞衰老,恢复视力 。
这不仅是一个普通的药物批件,这标志着哈佛大学遗传学教授、抗衰老领域的领军人物 David Sinclair 提出的“衰老信息理论”将迎来终极“大考” 。
这到底意味着什么?简单来说,科学家们不再满足于在小白鼠身上让它们变年轻了。这一次,他们要直接在人类身上按下“重启键”。这项基因疗法旨在使用一种能够改变 DNA 化学标签的技术(即表观遗传重编程),让老化的细胞“表现得”更年轻 。虽然试验的首要重点是安全性,但其核心目标是恢复青光眼及一种罕见眼病(NAION)患者的视力 。
Life Biosciences 此次抢在亚马逊贝佐斯投资的 Altos Labs 和 OpenAI 山姆・奥特曼投资的 Retro Biosciences 之前,率先进入人体试验阶段,无疑在这场关乎人类未来的竞赛中拔得头筹 。
你可能要问:这项技术到底是什么?它是如何工作的?为什么全球顶级富豪都在疯狂押注?
为了让你彻底读懂这一历史性事件背后的硬核逻辑,我们特意整理了一份详尽的深度研报。以下内容将带你从诺贝尔奖级的发现开始,一步步揭开“逆转衰老”的神秘面纱。
👇👇👇
长寿的表观遗传重编程:进展、挑战与未来方向
(Epigenetic Reprogramming for Longevity:Progress, Challenges, and Future Directions)
从山中伸弥的突破到逆转衰老
(From Yamanaka's Breakthrough to Aging Reversal)
现代长寿表观遗传重编程领域可以追溯到山中伸弥(Shinya Yamanaka)在 2006-2007 年对诱导多能干细胞(iPSCs)的开创性发现。山中伸弥鉴定了四个胚胎转录因子――Oct4、Sox2、Klf4 和 c-Myc,现在被称为“山中因子”(OSKM)。这些因子可以将成体细胞重置为类似胚胎的多能状态,有效地将它们的生物时钟倒拨回去 [1]。这场细胞生物学的革命为山中伸弥赢得了 2012 年诺贝尔奖的一部分,并证明了细胞的衰老并不是一条单行道。
科学家们意识到,仅通过重新激活这四个与年轻相关的基因,就有可能擦除细胞的表观遗传记录并将其恢复到“出厂设置” [2, 3]。这一发现提出了一个大胆的问题:我们能否利用这种内置的“重置”机制――不仅仅是在分离的细胞中,而是在活体生物体内――来对抗衰老?
【注:什么是“表观遗传”?】
表观遗传学(Epigenetics)是指 DNA 和组蛋白上的化学标签网络,它们像开关一样控制着基因的活动。想象 DNA 是钢琴的琴键,而表观遗传学就是决定弹奏哪首曲子的乐谱。
表观遗传学在衰老中起着关键作用。随着时间的推移,表观遗传代码会变得扭曲,导致细胞读取错误的基因并发生故障 [5]。山中伸弥的工作为生物学提供了一个“作弊码”:通过重置表观遗传标记,衰老的细胞可能会恢复活力。
在 2007 年之后的几年里,全世界的研究人员迅速看到了重编程在抗衰老方面的潜力,大量资金涌入该领域 [3]。这为一种新的长寿策略奠定了基础:表观遗传重编程――本质上就是将细胞的表观遗传时钟倒拨回更年轻的状态。
挑战:完全重编程是危险的
(The Challenge:Full Reprogramming is Dangerous)
尽管前景广阔,但将细胞完全重编程回 iPSC(诱导多能干细胞)状态作为一种衰老疗法是不可行的。
问题在于 OSKM(山中因子)会擦除细胞的身份――一个完全恢复到干细胞样状态的心脏细胞或神经元会“忘记”它的功能 [7]。在活体生物中,触发完全的多能性将是灾难性的,这类似于将体内许多细胞变成没有任何专门功能的胚胎细胞――这显然与生命存续不相容。
此外,山中因子中的一个,c-Myc,是已知的癌基因(oncogene)。研究发现,在成年小鼠体内持续表达 OSKM 会诱发畸胎瘤(含有头发和牙齿等组织的混合肿瘤),并经常因癌症生长导致死亡 [9, 10]。因此,不受限制的重编程会驱动不受控制的细胞增殖和肿瘤形成,以及因分化细胞丧失而导致的器官衰竭 [9, 11]。这些挫折强调了山中伸弥的“重置按钮”在体内使用之前需要一把“安全锁”。
研究人员很快发现了一个解决方案:部分重编程(Partial Reprogramming)。这个想法是激活诱导年轻的因子,其程度刚好足以使细胞的表观遗传组(epigenome)恢复活力,但又不足以使细胞失去身份或开始形成肿瘤 [12, 13]。在实践中,这意味着瞬时或周期性地暴露于重编程因子――开启它们一小段时间然后关闭――或者使用山中因子的一个子集。
值得注意的是,研究发现省略 c-Myc 可以显着降低癌症风险 [10, 14]。正如哈佛医学院的 David Sinclair 博士发现的那样,仅使用四个因子中的三个(Oct4、Sox2、Klf4――简称“OSK”)可以避免 c-Myc 的致癌作用,同时仍能重置许多衰老的表观遗传标记 [15, 14]。这种 OSK 方法成为了安全年轻化疗法的基础,Sinclair 将其比作从旧唱片上磨去划痕――细胞的“音乐”(基因表达)像新的一样播放,而无需更换唱片 [16]。
总之,部分重编程在疗效和安全性之间取得了平衡。通过仔细调节山中因子表达的程度和时间,科学家可以逆转表观遗传衰老标记并恢复细胞的年轻功能,而不会擦除细胞身份,也不会引发恶性生长 [13, 14]。这个概念――在不完全去分化(dedifferentiation)的情况下的年轻化――是当前表观遗传抗衰老策略的基石。
早期概念验证:让细胞和小鼠重返年轻
(Early Proof-of-Concept:Rejuvenating Cells and Mice)
在实现体内年轻化之前很久,就有迹象表明重编程可以在细胞水平上逆转衰老。
2011年,法国 Jean-Marc Lemaître 领导的一个团队证明,即使是极老的人类细胞也可以通过重编程恢复活力 [17, 18]。他们提取了老年捐赠者(包括百岁老人)的皮肤成纤维细胞,并引入了六个因子(OSKM 四重奏加上 NANOG 和 LIN28)。这些衰老的细胞被重置为 iPSC,然后重新分化;令人惊讶的是,这些“重生”的年轻成纤维细胞具有延长的端粒、健康的线粒体和与年轻细胞无法区分的基因表达谱 [18, 19]。这是第一个证据,证明衰老的体细胞可以恢复到更年轻的状态,在此过程中擦除了细胞衰老的关键特征 [19, 20]。它证明了在细胞水平上,衰老并非不可逆转的损伤积累――这是一个开创性的见解,尽管是在培养皿中实现的。
然而,真正的愿景是在活体动物中应用部分重编程来逆转衰老。开创性的突破来自 2016 年索尔克研究所(Salk Institute)的 Juan Carlos Izpisúa Belmonte 博士小组。
在一篇具有里程碑意义的《Cell》论文中,Ocampo 等人表明,在小鼠体内进行短期 OSKM 诱导的循环可以改善多种衰老特征,甚至延长寿命 [21]。他们使用了转基因小鼠(和一种早衰模型),这些小鼠带有一个可诱导的 OSKM 系统,可以间歇性地开启。
结果令人震惊:
来自早衰小鼠的细胞:当短暂暴露于 OSKM 时,开始在分子水平上看起来和表现得更年轻,且没有失去其皮肤细胞的身份 [22]。这些细胞中的关键衰老标记(积累的 DNA 损伤、异常的基因表达模式)得到了逆转 [22]。这确立了部分重编程可以在体内使细胞恢复活力。
在早衰小鼠中:OSKM 诱导的循环导致组织功能改善,并且与未治疗的对照组相比,寿命延长了 30% [21]。治疗后的小鼠表现出较少的衰老病理,并且尽管治疗方案中存在 c-Myc,但并未患上癌症 [21]。本质上,这些小鼠的衰老被减缓并部分逆转了。
令人兴奋的是,索尔克团队还测试了自然衰老(非早衰)的老年小鼠。部分重编程提高了它们的再生能力――例如,老年小鼠在 OSKM 治疗后恢复了更年轻的治愈受伤肌肉和胰腺组织的能力 [23]。接受治疗的老年小鼠比未接受治疗的同龄小鼠具有更好的器官功能,并且在生物学上显得更年轻 [21, 23]。
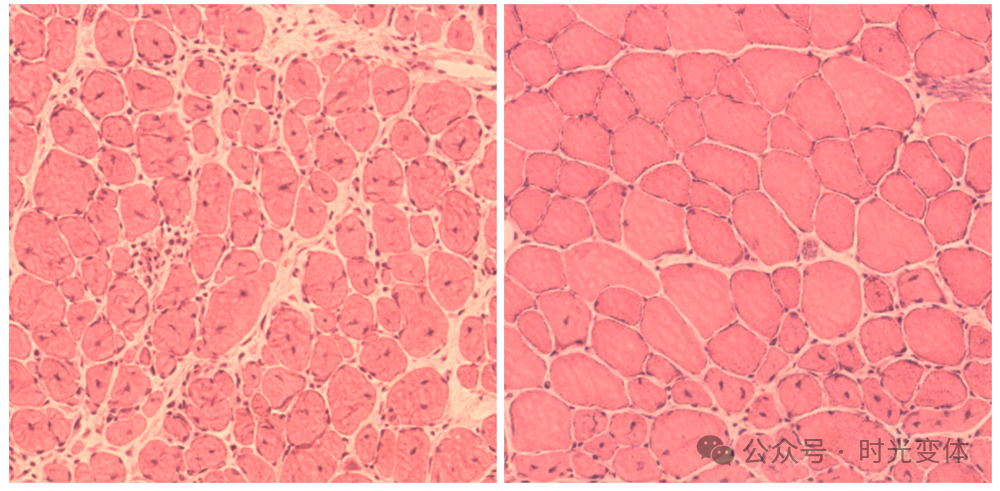
受损与改善的老年小鼠肌肉再生对比:左图显示再生能力差的老年小鼠肌肉,右图显示经过部分重编程治疗后的老年小鼠肌肉,具有显著改善的再生能力(更致密、更健康的肌纤维)。
Belmonte 2016 年的研究被广泛认为是衰老可以通过表观遗传重编程被靶向和逆转的概念验证。“我们的研究表明,衰老可能不必朝着单一方向发展……通过仔细的调节,衰老可能会被逆转,” Belmonte 说道 [24]。这表明即使在老年动物中,表观遗传组也具有高度的可塑性 [24]。重要的是,索尔克团队有先见之明地指出,对于人类治疗,直接使用基因可能有风险;他们指出化学物质或小分子诱导类似的表观遗传年轻化是一种有前途的替代方案――尽管这一方案可能需要十年的时间来开发 [25]。(截至 2026 年,这十年已经过去,确实,表观遗传重编程的首批临床试验现在正在开始,如下文所述。)
继索尔克研究之后,一波研究浪潮证实并建立在部分重编程用于逆转衰老的概念之上。2020 年,哈佛大学 David Sinclair 博士实验室的一个显著里程碑出现了。Sinclair 的团队专注于眼睛――特别是视网膜――作为中枢神经系统衰老的模型。在老年小鼠和患有青光眼的小鼠中,他们通过一种安全的 AAV(腺相关病毒)基因治疗载体,仅将 OSK 因子(去掉了 c-Myc)输送到视网膜细胞中 [26]。OSK 基因被置于一个可诱导的启动子下(由抗生素多西环素触发,以严格控制时间)。
发表在《Nature》上的结果非常显著:
接触 OSK 的衰老视网膜神经节细胞(眼睛的神经元),其 DNA 甲基化模式和基因表达谱被重置为更年轻的状态,有效地将细胞“重编程”为更年轻的生物学年龄 [27]。
在青光眼损伤的眼睛模型中(视神经纤维受损且视力丧失),OSK 治疗再生了神经轴突并在损伤后恢复了视力――这是以前很少见的壮举 [28, 29]。接受治疗的小鼠恢复了已丧失的视觉功能,证明了这是对年龄相关损伤的真正逆转(不仅仅是预防)[29, 28]。
在自然衰老的小鼠(12个月大,相当于人类中年)中,相同的治疗改善了随年龄下降的视力。衰老视神经中的电信号和分子信号开始类似于年轻小鼠的信号,并且接受治疗的老年小鼠的视觉表现变得敏锐 [30, 27]。
至关重要的是,Sinclair 的研究表明这可以在体内安全地完成。通过省略 c-Myc 并使用受控的、组织特异性的递送,他们避免了肿瘤或异常生长 [10, 14]。重编程的视网膜细胞没有失去其身份――它们没有变成胚胎干细胞或形成畸胎瘤。相反,它们只是变成了年轻版本的自己,重新获得了再生潜力。“我们的研究表明,可以安全地逆转复杂组织(如视网膜)的年龄并恢复其年轻功能,” Sinclair 说 [31, 32]。这是动物视力衰老的首次成功逆转,它强调了部分重编程可以是一种精确靶向的治疗干预,而不是一种全身性的风险。
本质上,到 2020 年,该领域已从一个有趣的小鼠寿命实验转变为一个实用的治疗范式:使用部分表观遗传重编程来治疗特定的年龄相关疾病(如青光眼或视力丧失),通过使受影响的细胞恢复活力。这为新一代生物技术公司将这些发现转化为人类治疗方法奠定了基础。
新兴格局:公司与竞争
(The Emerging Landscape:Companies and Competition)
鉴于表观遗传年轻化的巨大前景,大量资金和人才涌入这一领域也就不足为奇了。数十家生物技术初创公司(通常由科技亿万富翁支持)和研究机构正在追逐用于长寿的部分重编程方法 [3, 33]。值得注意的是,科学上存在显着的重叠――大多数参与者都建立在山中伸弥的工具包之上――但每一家都在方法论和目标上开辟了自己的细分市场。
以下我们概述了一些关键组织以及它们如何区分自己:
Life Biosciences(波士顿, 美国)
由 David Sinclair 联合创立,Life Bio 是专注于 OSK 基因疗法治疗年龄相关疾病的领跑者 [15]。他们使用 AAV 载体将 OSK 输送到特定组织,并配备药物诱导系统以严格控制时间(例如,使用多西环素开启基因几周,然后关闭)[34, 35]。Life Biosciences 的第一个目标是眼睛:在动物研究中,他们的治疗再生了被压碎的视神经并逆转了老年小鼠的青光眼 [36]。他们报告说,在 2023 年恢复了非人灵长类动物的视力 [37]――这是一个重要的里程碑――截至 2026 年初,他们正在启动针对眼部疾病患者的临床试验 [38, 39]。该公司本质上是在转化 Sinclair 的“OSK入眼”方法;他们称之为“部分表观遗传重编程”,并将其比作重启损坏的软件 [40]。Life Bio 的竞争优势在于强大的临床前证据基础(在啮齿动物和灵长类动物中)以及相对较近的临床时间表。
Altos Labs(旧金山湾区 & 全球)
Altos Labs 是一家于 2022 年成立的资金雄厚的研究机构,据报道拥有超过 30 亿美元的支持(特别是来自亚马逊的杰夫・贝佐斯),它招募了包括 Juan Carlos Izpisúa Belmonte 和山中伸弥本人(作为科学顾问)在内的顶级先驱 [41]。Altos 采取广泛的基础方法:探索如何通过部分重编程使整个组织和生物体恢复活力,同时避免完全的多能性 [42]。Altos 在美国、英国和日本设有业务,组建了一支全明星科学团队,深入研究表观遗传衰老和年轻化的机制。他们对具体的治疗目标不太公开,但有迹象表明他们旨在通过微调重编程过程(可能开发新型基因递送系统、药物鸡尾酒和体内使用的安全方案)来修复或再生多个器官 [42]。Altos 的竞争优势在于其专业知识和资金的绝对集中――它与其说是一家单一用途的生物技术公司,不如说是一所细胞年轻化的研究机构。值得注意的是,拥有山中伸弥指导研究(以非营利顾问身份)意味着 Altos 与 iPSC 技术的原始知识产权(IP)和专有技术有着深厚的联系 [43]。
Retro Biosciences(旧金山, 美国)
由 OpenAI 首席执行官 Sam Altman 支持(投资了 1.8 亿美元),Retro Biosciences 同样在追求逆转细胞年龄的疗法,尽管细节有些保密。Retro 强调采用 AI 驱动的方法 来优化重编程因子和方案 [44, 45]。据报道,他们正在筛选因子的许多组合和条件,以找到最安全、最有效的方法来使细胞恢复活力(“细胞年龄重编程”)[46, 47]。Retro 对血液因子和血浆置换也表示了兴趣,但在重编程领域,他们使用机器学习(“发现引擎”)来大规模测试部分重编程干预措施 [46]。该公司最近宣布计划筹集超过 10 亿美元用于开发,目标是在 2025 年左右进行人体试验 [48]。虽然他们具体的治疗目标尚未公开,但 Retro 的理念是广泛探索(多种细胞类型和因子),然后将最有希望的年轻化策略推向临床。这种高通量、计算引导的策略使 Retro 与众不同,可能会产生超越标准山中因子集的新因子组合 [49]。
NewLimit (旧金山湾区, 美国)
由科技企业家 Brian Armstrong 于 2021 年联合创立,NewLimit 明确专注于表观遗传年轻化以延长人类寿命。NewLimit 的方法集中在高通量筛选和表观遗传编辑上,以发现倒带细胞年龄的新方法 [46, 47]。他们的团队正在人类细胞中测试无数的转录因子组合,并使用机器学习衰老时钟来查看哪些“鸡尾酒”使老细胞看起来年轻 [47]。有趣的是,NewLimit 报告说他们发现了许多山中四因子之外的因子可以使细胞恢复活力――这意味着拥有专有的新靶点 [49]。他们还有一个“编写团队”致力于表观遗传编辑工具(可能基于 CRISPR),以直接重置表观遗传标记 [50]。虽然仍处于临床前阶段,但 NewLimit 的雄心是开发无需基因疗法即可恢复年轻状态的疗法,可能是通过 mRNA 递送或小分子。他们的竞争优势在于这条发现管线,它可能通过找到更简单或更有针对性的重编程方法来超越该领域。截至 2024 年年中,他们已证明免疫细胞的“表型年龄”发生逆转,并正在扩展到其他细胞类型 [47, 49]。
Turn Biotechnologies(加利福尼亚, 美国)
作为一家采用非病毒、瞬时基因治疗路线的初创公司的例子,Turn Bio 的 ERA™ 平台使用修饰的 mRNA 短暂地递送 OSK(有时是其他因子)[51, 52]。mRNA 的半衰期很短,允许精细控制――因子瞬时表达然后降解,降低了过度重编程的风险。2020 年,Turn Bio 的学术创始人(Sebastiano 等人)表明,山中因子 mRNA 的脉冲可以在培养物中使细胞恢复活力而无需基因组整合 [53]。Turn 最初将其应用于皮肤和软骨的年轻化。这种 mRNA 方法是病毒载体的一个有吸引力的替代方案:它避免了插入突变,并且可以重复给药。Turn 的竞争利基在于专注于部分重编程的局部、美容或肌肉骨骼应用(例如再生皮肤、通过使软骨细胞恢复活力来治疗骨关节炎),使用易于控制的 mRNA 递送 [51]。
其他公司和学术界
除上述之外,许多其他实体也在参与竞赛。例如,Calico Life Sciences(谷歌的抗衰老公司)有关于表观遗传衰老的项目,尽管它们在方法上更加隐秘和广泛 [48]。学术界非常活跃:像英国的 Shift Bioscience 这样的团队使用 AI 来寻找安全的基因鸡尾酒,这些鸡尾酒可以在不进行完全重编程的情况下逆转细胞衰老 [54, 55]。大型联盟和政府倡议(包括在中国的,将在后面讨论)也在投资表观遗传年轻化。在这个阶段看到合作而不是公开竞争是很常见的――例如,Altos Labs 聘请了领先的学者并鼓励发表论文,Life Biosciences 拥有多个大学合作伙伴关系。许多科学家在多家公司担任顾问,知识通过会议和出版物相对自由地流动。该领域仍处于探索阶段,验证科学是比担心市场份额更重要的优先事项。
鉴于这种格局,人们可能会问:这些参与者是否正处于知识产权(IP)或市场竞争的冲突路线上?
到目前为止,这种重叠并未导致公开冲突。所有人都使用山中因子的某种变体,但山中伸弥的核心 iPSC 专利不再是障碍――2006 年的基础专利(US8058065)将于 2026 年左右到期,有效地使山中因子的获取民主化 [56]。(事实上,这些专利曾通过京都大学的 iPS Academia Japan 征收昂贵的许可费;它们的到期预计将刺激创新并降低每个人的成本 [56]。)新的专利已就具体的实施方式提交――例如,Sinclair 及其同事为他们的 OSK 基因治疗方法申请了专利,Life Biosciences 已为其项目许可了该 IP [57]。其他公司已就其平台发现的化学鸡尾酒或新因子申请了专利。然而,这些专利往往是狭窄的(特定的载体、特定的因子组合或用途)。截至 2026 年初,没有任何迹象表明部分重编程公司之间存在任何专利侵权诉讼或“专利战”。相反,该领域似乎意识到如果科学成功将带来的巨大机会,并存在一种谨慎合作的氛围。重叠的人员和顾问(例如 Yamanaka 为 Altos 提供咨询,Sinclair 的学生在 Life Bio 工作等)也促进了协作环境。
总之,每家公司都开辟了自己的 IP 领地(递送方法、特定的基因调整、疾病目标),并且随着基本工具的广泛可用,进展更多地是由执行和数据驱动的,而不是排他性。只要每个人都面临共同的科学障碍(安全性、递送、疗效),人们就会感觉到在长寿生物技术领域“水涨船高”。
监管和法律考量(美国与中国)
(Regulatory and Legal Considerations(U.S. & China))
表观遗传年轻化疗法通往临床应用的道路既关乎生物学,也关乎监管科学和政策。
在美国,一个主要的考量是衰老本身尚未被 FDA 承认为一种可治疗的疾病。长寿干预措施的开发人员目前无法获得“抗衰老”或“逆转衰老”本身适应症的药物批准 [58]。相反,公司必须针对特定的年龄相关疾病或状况。这在 Life Biosciences(将青光眼/视力丧失作为首个适应症)和其他选择离散疾病(例如老年患者的心血管疾病、骨关节炎等)的策略中显而易见。衰老研究界也在平行努力(例如二甲双胍的 TAME 试验)以说服监管机构可以将衰老视为一种“适应症” [59],但在那发生之前,表观遗传重编程疗法可能会首先被批准用于狭窄的适应症,然后可能被超说明书用于更广泛的年轻化。
FDA 将在基因疗法或先进生物制品的框架下审查这些疗法,这意味着安全性至关重要。关键问题包括:基因组整合(对于 DNA 载体)、对病毒载体的免疫反应、致瘤性以及对细胞的脱靶效应。到目前为止,临床前结果令人鼓舞――例如,Sinclair 在小鼠身上的 OSK 疗法显示癌症或其他病理变化没有增加 [11, 14]。尽管如此,人体试验可能会非常谨慎地开始(例如,局部递送至一个器官、瞬时表达、彻底监测)。FDA 拥有基因疗法甚至 CAR-T 等细胞疗法的经验,但表观遗传年轻化可能会引发独特的问题:你如何衡量作为益处的“生物学年龄”改善?什么是可接受的终点(功能改善、生物标志物、表观遗传时钟逆转)?监管机构可能要求证据证明干预措施不仅仅使细胞在指标上变年轻,而且实际上转化为更健康的组织功能和疾病缓解,这正是早期动物研究旨在证明的 [60, 61]。
从美国的知识产权和指导方针的角度来看,如前所述,随着专利到期,山中因子的操作自由度正在扩大。一些先行者(哈佛、索尔克等)拥有关于重编程方法的专利资产,但许多是开放或许可的。展望未来,监管指南也将决定什么是可行的――例如,FDA 可能会要求任何基于基因疗法的年轻化必须是可诱导的或受控的,作为一种安全开关(我们已经看到公司建立了多西环素开启/关闭开关 [34])。鉴于逆转衰老的新颖性,可能还会有关于试验参与者年龄的指导方针(在老年人与中年人中进行测试)。
在中国,格局正在动态演变。中国面临着向老年人口的巨大人口转变,近年来已将健康老龄化提升为国家战略重点 [62, 63]。自 2024 年以来,中国当局一直在高层支持“长寿产业”倡议、再生医学和延长寿命的生物技术 [63]。这种政策环境意味着中国的监管机构可能对抗衰老试验持接受态度,在设计上可能更加灵活,尽管中国的 FDA(NMPA)仍然适用严格的安全标准。
重要的是,中国科学家以大胆的年轻化实验登上了头条新闻。2025年,中国科学院刘光慧(Guanghui Liu)领导的团队在《Cell》上发表了一项开创性研究,展示了灵长类动物衰老的逆转――这是在亲缘关系密切的物种中的首次此类演示 [64, 65]。他们没有使用 OSK 基因疗法,而是对人类间充质祖细胞进行了基因工程改造,使其具有抗衰老性并分泌年轻化因子,然后将这些细胞输注给老年猕猴 [66]。在 44 周的时间里,接受治疗的猴子表现出多系统的功能改善:更好的肌肉和骨骼强度、改善的认知功能、年轻化的卵巢和神经元,以及衰老的分子标记倒退了相当于几年的时间 [67, 68]。值得注意的是,没有肿瘤或不良反应,关键的抗衰老益处归因于移植细胞释放的外泌体(exosomes),这些外泌体减少了炎症并重置了天然细胞中的表观遗传程序 [69]。这项研究强调了中国的承诺以及一种不同的方法――利用细胞疗法和分泌的囊泡来诱导表观遗传重启。
【注:外泌体 Exosomes】
细胞分泌的小囊泡,就像细胞之间传递的包裹,里面装着蛋白质、RNA等信号分子。在这里,它们就像是年轻细胞发出的“青春信号包”。
在监管方面,中国过去曾批准过干细胞试验,并且可能会通过快速通道审批针对衰老疾病的疗法,特别是如果与这种国内研究成功相关联的话。
在法律上,中国也在扩大生物技术的专利保护,我们可以预期中国机构和公司将就其开发的任何新颖的重编程因子或方法申请专利。例如,如果中科院团队的“抗衰老细胞”或其外泌体因子是独特的,那些可能是专有的。我们尚未看到该领域中西方实体之间的公开专利纠纷,这可能是因为该领域还很年轻,重点是首先在临床上证明概念。事实上,存在美中合作的潜力――衰老是一个全球性问题,中国的试验或数据可以补充西方的努力。尽管如此,每个国家的监管路径可能不同:如果不进行广泛的安全数据,美国可能会较慢地批准大胆的年轻化试验,而鉴于对健康老龄化的战略重视,如果早期结果有希望,中国可能会尝试更大规模或更加速的试验。
总之,美国和中国都在走向拥抱表观遗传重编程,但框架不同。美国依靠私人生物技术创新和谨慎的监管,从疾病开始,如果有证据支持,可能会转向将衰老作为一种适应症。中国将国家驱动的研究与政策支持相结合,可能允许更快地从实验室过渡到临床(如猴子研究所见)。在两个司法管辖区,2026-2030 年将是一个关键时期,监管机构、伦理学家和科学家将敲定这一类新药物――逆转衰老疗法――的指导方针。
未来展望:超越病毒载体与其他表观遗传疗法
(Future Perspectives:Beyond Viral Vectors and Additional Epigenetic Therapies)
当前的生物技术长寿浪潮仅仅是个开始。虽然使用 OSK 的基因疗法是体内部分重编程的第一个可行方法,但研究人员正在积极开发非病毒和非遗传的方法来实现类似的年轻化,这可能更安全、更具可扩展性并且适用于全身。
几个有前途的途径即将出现:
用于年轻化的化学鸡尾酒(Chemical Cocktails):
一个主要问题是我们是否可以用药片代替基因来倒拨表观遗传时钟。就在最近,在鉴定模仿山中因子作用的小分子方面取得了突破。2023 年,Sinclair 实验室的一个团队报告了一组六种化学鸡尾酒,当应用于培养中的老年人类细胞时,在一周内使其恢复了年轻状态 [70]。这些鸡尾酒恢复了年轻的基因表达模式,并通过表观遗传指标逆转了细胞的转录组年龄,而没有改变细胞身份 [71]。换句话说,他们在体外实现了 OSK 基因疗法所做的,但是使用的是药物而不是基因插入。这项具有里程碑意义的研究证明了纯化学重编程是可能的 [70, 72]。这些鸡尾酒可能针对汇聚在表观遗传状态上的关键信号通路和染色质修饰因子(可能的成分包括 HDAC 抑制剂、DNA 甲基化调节剂、代谢化合物等,尽管具体细节仍是专有的)。这意味着深远的意义:在未来,人们可能会服用口服药物组合或注射药物鸡尾酒一小段时间,以使全身细胞恢复活力。当然,这些结果处于细胞培养阶段;下一步将是在动物身上进行测试,看看化学重编程是否可以在体内安全地逆转衰老。但是公司已经在组建以改进这些鸡尾酒。Life Biosciences 的 CEO 提到,在他们的基因疗法成功后,他们设想转向小分子进行全身年轻化 [73, 74]。这种药物可以克服基因疗法的分布问题(目前必须单独递送到每个目标组织 [75])。一种能“重置”多个器官表观遗传组的系统性药物有点像圣杯――可能实现全身年龄逆转。实现特异性并避免癌症将是关键挑战(药物可能比靶向基因表达更钝),但早期数据令人鼓舞,即可以以可控的方式化学诱导部分重编程 [71]。
mRNA 和类 mRNA 递送:
mRNA 疫苗的成功促进了对将 mRNA 用于其他疗法的兴趣。正如 Turn Biotech 所指出的,编码 OSK 的修饰 mRNA 分子可以被递送到细胞,导致它们瞬时产生重编程因子,然后自然降解。这种方法不留下永久性的遗传改变(mRNA 不整合到 DNA 中),并且可以随意重复给药或停止。它有效地为细胞提供“软件更新”而不改变硬件。公司正在努力提高 mRNA 的稳定性和组织靶向性(例如,将 mRNA 递送到某些器官的脂质纳米颗粒)。另一种变体是自扩增 RNA 或环状 RNA,它们可能表达时间稍长但仍不整合。mRNA 方法可以大大简化制造(不需要病毒生产)并减少与基因组修饰相关的监管障碍。关键在于将足够量的 mRNA 递送到正确的细胞――这是正在积极研究的内容,借鉴了肿瘤学和疫苗递送的创新。
蛋白质或肽递送:
更具未来感但也并非不可想象的是递送诱导重编程的蛋白质或肽。转录因子是不容易穿过细胞膜的大蛋白质,但通过先进的蛋白质工程或细胞穿透肽,人们可以设想直接递送因子。或者,可能会发现激活细胞自身山中因子基因的小分子――实际上是一种间接方式,让细胞从其基因组中瞬时表达 OSK,而无需基因疗法。例如,可以使用 CRISPR 激活(CRISPRa),其中 dCas9 蛋白加向导 RNA 原位靶向 Oct4/Sox2/Klf4 的启动子,暂时开启它们。这将是一种诱导可逆重启的基因组编辑方法。虽然复杂,但早期研究表明,靶向表观遗传编辑(例如使用融合到去甲基化酶的 dCas9)可以实现特定衰老标记的年轻化 [76, 46]。
细胞疗法和分泌因子:
中国的灵长类动物研究强调了一种不同的范式:使用活细胞作为年轻化信号的“工厂”。与其改变体内的每一个细胞,不如设计一群细胞(例如干细胞),让它们不断向身体分泌年轻信号(外泌体、生长因子、miRNA)。猴子实验中使用的抗衰老祖细胞(SRCs)分泌的外泌体被动物的细胞摄取,从而间接重编程了它们的表观遗传状态 [69]。这表明细胞疗法可以在不在每个组织中进行基因治疗的情况下系统地传达表观遗传重置。公司可能会探索储存经过修饰以安全分泌此类因子的通用供体细胞(确保它们不会过度生长或形成肿瘤),并将它们作为一种输液用于衰老患者。外泌体本身甚至可以被分离出来并用作无细胞疗法。虽然仍处于实验阶段,但这种“细胞分泌的年轻化”方法令人信服,因为外泌体可以循环并穿透许多组织。
其他表观遗传药物:
除了重编程因子外,任何针对表观遗传调节酶和通路的药物都可以被视为衰老的表观遗传疗法。例如,像白藜芦醇或 NAD+ 增强剂(NR, NMN)这样的 Sirtuin 激活化合物(STACs)旨在增强 SIRT1,这是一种去乙酰化酶,有助于维持年轻的染色质并与动物寿命延长有关。虽然不如 OSK 显着,但这些对基因表达有适度的影响,并且正在针对年龄相关疾病进行测试。组蛋白去乙酰化酶(HDAC)抑制剂和 DNA 甲基化抑制剂用于癌症,可能有助于重新激活衰老细胞中沉默的年轻基因――尽管粗暴使用可能有风险。研究人员正在尝试设计选择性的表观遗传调节剂,例如,去除与衰老相关的异常甲基化标记或增加随年龄增长而关闭的区域的染色质可及性。一个例子是 TET 酶激活剂(因为 TET 蛋白主动去甲基化 DNA,并被证明是 OSK 驱动的年轻化所必需的 [77])。另一个领域是染色质重塑因子――例如,异染色质(结构性 DNA 包装)的丧失是衰老的一个特征,因此支持异染色质或纠正组蛋白水平的药物可能会对抗衰老的各个方面。这些更传统的药理学策略可能无法单独逆转衰老,但可以补充重编程或解决特定的衰老特征(例如,提高基因组稳定性或减少衰老)。
组合疗法以产生协同效应:
归根结底,衰老是多方面的。表观遗传重编程解决了表观遗传改变这一特征,并可以重置许多系统,但它可能无法修复积累的 DNA 突变或去除已经存在的衰老细胞 [78, 79]。未来的长寿治疗可能会结合多种方法。我们可能会看到一种治疗方案,患者首先接受 Senolytic(一种清除导致炎症的衰老“僵尸”细胞的药物 [80]),然后是表观遗传年轻化疗法使剩余细胞恢复活力,也许还有基因疗法来纠正任何显性负突变。事实上,Senolytic 药物(如 Unity Biotech 的 UBX1325)和基于 CRISPR 的基因疗法已经在针对特定的衰老疾病进行试验 [80, 81]。这些并不能直接重置时钟,但可以减轻损害。从长远来看,全面的抗衰老治疗策略可能涉及定期的部分重编程“调整”(定期恢复年轻的基因表达和功能,也许每十年一次),并结合维持疗法(管理新陈代谢、清除衰老细胞等)。
当我们展望未来时,几个关键挑战仍然存在。递送是一个大问题:到达人体的所有细胞远比在小老鼠身上难。目前的基因治疗载体无法均匀地转导每个器官 [75]。小分子可以,但必须确保特异性,以避免意外重编程(例如生殖细胞)或促进癌细胞。安全监测将至关重要――也许将通过频繁的活检或液体活检来跟踪患者,以确保没有细胞开始表现出不需要的去分化迹象。另一个挑战是在人类中测量年轻化。我们将需要可靠的生物学年龄生物标志物――例如表观遗传时钟读数、转录组年龄、蛋白质组学特征――以了解疗法是否真的使人在生物学上更年轻 [59, 82]。幸运的是,这个生物标志物领域正在迅速发展(甲基化时钟、GrimAge、DunedinPACE 等,有些甚至用于初步试验)。监管机构接受此类生物标志物作为替代终点将大大加快开发速度。
结论
(Conclusion)
总之,始于山中伸弥四个基因的概念已发展成为长寿科学的核心支柱。在短短 15 年里,我们已经从在培养皿中重编程细胞发展到在哺乳动物中使眼睛恢复活力并延长寿命。部分表观遗传重编程有力地证明了衰老是可塑的――这可能是一种可以治疗的疾病,而不仅仅是一种必然性。
接下来的十年将决定我们在人类身上应用这一技术的程度。随着临床试验的开始以及改进方法(化学、mRNA 等)的平行努力,人们对表观遗传疗法可能开启衰老再生医学的新时代持谨慎乐观态度。正如 Andrew Steele 博士所沉思的那样,细胞重编程感觉像是“从未来通过虫洞掉下来的技术” [83]――然而我们就在 2020 年代,开始运用它。将这项技术安全有效地转化出来的竞赛正在进行中,这样也许有一天,曾经“不可避免”的衰老方面将成为可选项。
参考文献:
[1] Yamanaka, S., et al.(2006). "Induction of Pluripotent Stem Cells from Mouse Embryonic and Adult Fibroblast Cultures by Defined Factors." Cell.
[2, 3] Recent scientific literature and press releases on epigenetic reprogramming breakthroughs.
[5] Epigenetic mechanisms in aging.
[7] Cell identity and reprogramming risks.
[9, 10] Abad, M., et al.(2013). "Reprogramming in vivo produces teratomas and iPS cells with totipotency features." Nature.
[11] Organ failure risks in reprogramming.
[12, 13] Ocampo, A., et al.(2016). "In Vivo Amelioration of Age-Associated Hallmarks by Partial Reprogramming." Cell.
[14] Lu, Y., et al.(2020). "Reprogramming to recover youthful epigenetic information and restore vision." Nature.
[15, 16] Sinclair, D.A. & LaPlante, M.D.(2019). "Lifespan:Why We Age―and Why We Don't Have To."
[17, 18, 19, 20] Lapasset, L., et al.(2011). "Rejuvenating senescent and centenarian human cells by reprogramming through the pluripotent state." Genes & Development.
[21, 22, 23] Salk Institute Studies on Progeria and Aging Reversal(2016).
[24, 25] Izpisua Belmonte, J.C. commentaries on in vivo reprogramming.
[26, 27, 28, 29, 30] Lu, Y., et al.(2020). Nature cover story on vision restoration.
[31, 32] Press releases from Harvard Medical School(2020).
[33] Biotech investment landscape reports(2022-2025).
[34, 35, 36] Life Biosciences technical publications and pipeline updates.
[37, 38, 39] Life Biosciences primate study announcements(2023)and clinical trial launch(2026).
[40] Corporate presentations by Life Biosciences.
[41, 42, 43] Altos Labs launch details and scientific advisory board announcements.
[44, 45, 46, 47] Retro Biosciences and NewLimit blog updates(2024-2025).
[48] Investment news regarding Retro Biosciences.
[49, 50] NewLimit scientific updates on novel factors and epigenetic editing.
[51, 52, 53] Turn Biotechnologies publications on mRNA reprogramming(Sebastiano et al.).
[54, 55] Shift Bioscience research.
[56] Patent landscape analysis regarding Yamanaka factors expiry.
[57] Patent filings by Harvard and Life Biosciences.
[58, 59] FDA regulatory framework discussions on aging as an indication.
[60, 61] Clinical trial design considerations for longevity.
[62, 63] China's national strategic priorities on healthy aging.
[64, 65, 66, 67, 68, 69] Chinese Academy of Sciences study on primate aging reversal(2025)published in Cell.
[70, 71, 72] Yang, J.H., et al.(2023). "Chemically induced reprogramming to reverse cellular aging." Aging.
[73, 74] Interviews with Life Biosciences leadership.
[75] Delivery challenges in gene therapy.
[76] Epigenetic editing advances(CRISPRa/dCas9).
[77] Role of TET enzymes in reprogramming.
[78, 79, 80, 81] Combination therapies and senolytics(Unity Biotech, etc.).
[82] Biomarkers of aging(clocks).
[83] Steele, A.(2020). "Ageless:The New Science of Getting Older Without Getting Old."

















