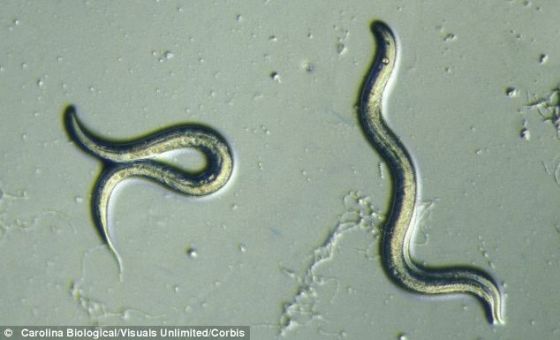
美国研究人员稍微调整实验室蠕虫――秀丽隐杆线虫的两个基因通路,使这种动物的寿命增加5倍。

科学家说,如果延长蠕虫生命的科学应用到人类身上,我们活到500岁就不会是个梦。这两个基因突变启动延长寿命的特定组织的正反馈循环。从根本上说,这些蠕虫可以活到相当于400到500年的人类寿命。

虽然还需多年研究才能显著延长人类生命,但这项研究增加通过遗传相互作用进行抗衰老治疗的可能性。
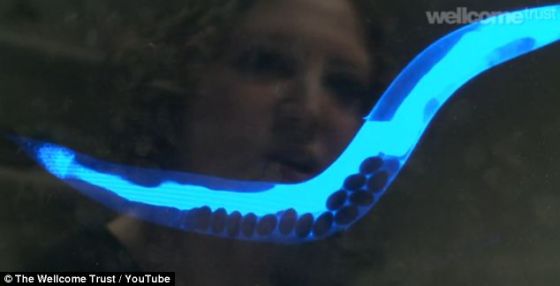
照片显示,在显微镜下很容易看到一段蓝色荧光穿过蠕虫内脏时的死亡蔓延。这种荧光由细胞坏死造成,它在有机体内的传播依赖于钙传递信号。
、科学家认为,如果延长蠕虫生命的科学应用到人类身上,我们活到500岁就不会只是一个梦想。美国研究人员稍稍调整了一下实验室蠕虫――秀丽隐杆线虫的两个基因通路,便使这种动物的寿命延长了5倍。他们表示,这项研究通过遗传相互作用得出的结果,让抗衰老疗法出现了令人期待的美好前景。
美国加利福尼亚州诺瓦托市巴克衰老研究所首席科学家潘卡基-卡帕西表示:“我们的实验证明蠕虫寿命增加了5倍。这两个基因突变启动延长寿命的特定组织的正反馈循环。从根本上说,这些蠕虫可以活到相当于400到500年的人类的寿命。”
这位科学家说:“虽然还需多年研究才能大大延长人类生命,但这项研究增加这项研究通过遗传相互作用得出的结果,让抗衰老疗法出现了令人期待的美好前景。在早年,癌症研究人员关注单基因突变,但后来发现一类基因的不同突变推动疾病过程。相同的事很可能发生在衰老上。”
秀丽隐杆线虫是第一种完整遗传密码被科学家绘制成图的动物,广泛应用于衰老和寿命研究中。《细胞报告》杂志刊登了这项新研究。在研究中,科学家抑制影响胰岛素活性和营养信号通路――雷帕霉素标靶的关键分子。
雷帕霉素标靶通路的单一基因突变使秀丽隐杆线虫寿命延长30%,但胰岛素信号传递突变使它们的寿命增加一倍。如果同时使用这两个方面,它们的寿命可能延长130%,但它们结合起来的效果更大。
这项研究可以解释难以识别使百岁老人长寿的单基因的原因。卡帕西表示:“对那些健康长寿的人来说,基因间的相互作用很可能是至关重要的。”科学家将来会对老鼠进行试验,看看哺乳动物是否也有同样的效果。卡帕西说:“我们的想法是用转基因老鼠抑制胰岛素传递信号,然后用雷帕霉素治疗它们。众所周知,这种药物具有抑制雷帕霉素标靶通路的作用。”

















