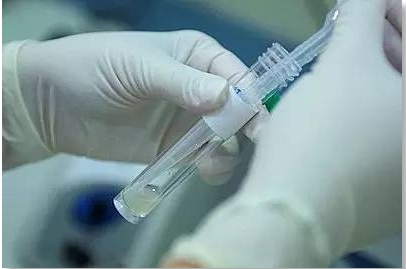
近日,法国里昂一家Kallistem(卡利干细胞)生物科技公司研究人员宣称,他们从6个患有不育症的男性睾丸中提取出精原细胞,成功培育出成熟的人造精子细胞。假若这一项技术真的成熟,而且卵子也接受,会带给人类哪些福音呢?是否会危及男性地位?
在过去20多年里,科学家一直尝试在实验室培养“人造精子细胞”。对于这次的研究成果,英国《独立报》称,这一消息在医学界引起轰动,但不少西方媒体对新成果态度谨慎,称这一重大“医学突破”仍需验证。
进行72天旅程的人造精子
Kallistem公司CEO在接受采访时说:“Kallistem正致力于解决影响世界各国面临的主要问题:男性不育治疗。我们团队开发了世界首个允许在体外获得完全成形的精子所需的技术。”
Kallistem公司成立于2012年,团队成员基本都是生物学博士。他们花了15年时间,才让原本不成熟的细胞慢慢变成成熟精子。

其实,精子的生成技术相当复杂。为了完善技术提高精子产量,此方法涉及到提取曲细精小管内的悬液,是一种叫壳多糖的胶状物。把提取液置于富含营养素、 维生素、 激素和生长因子的培养皿中,把培养皿放置在生物反应器内。Kallistem公司研究人员声称,精子生成这个过程在人体内完成需要72天时间,直到脱离曲细精小管,胶状物溶解,精子发育成熟。
此前,他们只在小白鼠身上做此实验,如今他们第一次在人类细胞上实验成功,顺利的话,1年后他们将完成前临床实验。如果实验成功,那么2017年他们便可利用临床实验让不孕患者生出孩子。他们会取出从男性的睾丸中取出尚未成熟的精原细胞,然后转换遗传物质形成成熟的精子,并利用试管做出宝宝。如果患者还不打算当爸爸,那他可以选择把精子先冷冻保存起来。
来自日本的研究团队早在2011年就成功地在实验室造出了小鼠精细胞,但法国研究者强调说,他们是世界上第一个进行人体实验的国家。该公司官网也详细介绍了制造“人造精子”的步骤。这一流程分为五步。首先,对因罹患睾丸癌或者其他原因导致不育的男孩和成年男性进行睾丸组织穿刺,提取干细胞。然后,将干细胞进行冷藏保存,在培养皿内把胚芽细胞培养成成熟的精子细胞;第三步,在模拟人体环境的“生物反应器”内将成熟的精子细胞低温贮藏起来;第四步,从体外将精子注入体内;第五步,怀孕。
“人造精子”的过程听起来非常“高大上”,难以理解。从精原细胞培育出了精子细胞,这项技术可行吗?美国生物学博士夏志告诉记者,“将精原细胞培育成精子细胞,并不是一个太大的问题。精子细胞是由精原细胞复制,减数分裂得来的。精原细胞属于雄性生殖细胞的早期阶段。用精原细胞培育成精子细胞,就是把自然界的此过程人工化,是人类操纵自然生命早期过程的科学体现,是技术进步。”
如果试验成功,公司希望通过人造精子,可以帮助患生殖系统癌症的年轻男性成为父亲,简单来说就是不孕不育症患者的福音。该公司在官网介绍称,这一技术将适用于1.5万名年轻的癌症患者,或者12万成年不育的男性,他们无法通过现有的试管婴儿技术来解决不孕症的困扰,“这一突破开辟了一条新的道路,这是被临床医生期待已久的治疗途径。”
人体验证效果还需要若干年
看到这里,诸多男同胞可能会长呼一口气,因为法国这项研究中的精原细胞还是由男性来提供,把它培育成精子细胞。
那么,精子细胞和精子是一回事吗?精子细胞能被培育成成熟的精子吗?夏志说,“精子细胞和精子不是等同的。精子细胞是精子的早期阶段,还要通过变形,如顶体发生,尾部发育,细胞质浓缩等过程。对此过程的了解及具体机理不够深入,是造成精子形成问题种种且成功率不够高,后续产生后代生存率低等问题的主要原因之一。”

此次研究在小白鼠身上获得成功,那么通常在动物身上的试验成功,就可以成功用到人体上吗?要经历一个怎样的阶段呢?“从动物实验过渡并运用到人体上,是一个极其漫长的过程。在这一点上,社会大众及各种新闻报道极容易混淆两者界限,会觉得‘动物可以了,人还会远吗?’把这两者等同看待,这样看待是不对的。”夏志解释,“人类作为极其复杂的高等动物,其生命机制及生理调控过程都是与其他动物大不同,且更为纷繁复杂,更易造成重大不良后果和影响的。一般来说都是先模式动物实验,常见的有小鼠,斑马鱼,然后再过渡到离人相对近缘的动物,如狗、猪、猴子身上,最后再开始在人体上进行一二三期试验,来验证并探究其效果,及其可能的不良反应等。”
事实上,这项技术用于对动物保护同样具有很大的价值,在大型野生动物日益稀少的今天,通过该技术能够有效地使一些珍稀雌性动物在缺乏雄性个体,或是雄性个体精子质量严重下降时,进行精子再造实验,使雌性个体受孕、繁殖,延续这一物种的数量。
全球研究具备生殖能力的精子
从长远来看,研究者们花费了巨资,来进行这项看似非常有意义的研究。但是,尽管该公司对自己的成果十分自信,但学界依然对这一成果产生了质疑。近年来,有关人造精子的研究,每隔一段时间就会出现类似研究的一个新进展,但最后的研究成果都不得而终。
2010年,英国《每日邮报》报道称,英国科学家想从女性捐赠者的骨髓中提取干细胞,然后利用特殊的化学药品将它们变成精子。这似乎意味着,女性也可以变相产生“人造精子”,从而使男性完全成为多余。尽管这一研究在发布时信心满满,称“女性精子”两年内就能面世,但5年过去了,这一结果并没有向外界发布。
2011年2月,发表在《自然》杂志上的一项研究中,日本横滨城市大学的生殖生物学家Takehiko Ogawa领导的研究人员摘除了出生两三天的幼鼠的睾丸,将这些睾丸置于一个含有专用培养基。随后,研究人员便任由这些睾丸生长。大约1个月后,研究人员注意到这些睾丸看起来相当正常并且正在产生精子。研究人员提取了精子并对雌鼠进行了人工授精,当时,受孕的雌鼠已产下12只健康的小鼠。利用相同的方法,研究人员甚至能够让已经冷冻了1个月的年轻睾丸产生精子。当时专家认为,这项技术对于治疗雄性不育具有重要意义。
据英国《每日电讯报》网站报道,2012年1月3日,德国和以色列科研人员从老鼠睾丸内提取了控制精子生成的生殖细胞,然后将其放在由琼脂胶构成的一种特殊化合物中,以创建与精子在睾丸内生长所相似的环境,最终成功培育出具备生殖能力的健康精子。当时,他们认为,这一技术有朝一日能帮没有生殖能力的男性实现“父亲梦”。
中国人造精细胞技术位居前列
值得一提的是,让人类感到不可思议的事实是,我们的生殖技术在不断地进步的同时,全球各地的男性精子质量却在普遍下降。有数据显示,美国不孕不育夫妇在10%-15%左右。这一比例在英国更高,约1/6的夫妇有生育困难问题,中国在这方面表现如何呢?
每年10月28日是男性健康日。根据相关文献及2015年全国男科年会公布的数据显示,上海志愿捐精者的合格率不超过21%,河南精子库捐献合格率为22%,北京合格供精者仅15%,我国男性精子质量每年下降1%以上,数量降低30%,每100对夫妇中至少有10对以上不能生育……
中国在人造精细胞研究领域也走在了世界前列。2015年7月10日,来自中科院上海生命科学研究院的研究员李劲松研究团队,成功建立了稳定的“类精子细胞”单倍体细胞系,这些细胞是利用幼年雄鼠体细胞克隆出来的,这些“类精子”能稳定地与雌鼠的卵细胞结合,产生出半克隆小鼠。相关研究发表在权威学术期刊Cell Stem Cell上。由于小鼠研究在人类的健康以及癌症研究等方面有很大的作用和参考价值,这些具有稳定遗传的半克隆小鼠自然意义非凡。
对实验动物来说,20%的健康后代或许已经足够好,但在人类身上就不行了,”李劲松研究员说,“如果该技术用在人类精子上,会导致出生时有80%会死亡或有缺陷。”
早在2012年,李劲松团队宣称将一个精子放入一个已经移除了细胞核和遗传物质的卵细胞中。结果该实验获得了一个类似胚胎细胞的干细胞,具有类似精子的功能,但没有尾巴,无法游动。这种干细胞可以用来大批量生成类似的人工细胞。不过,该技术目前的效率还很低,获得的受精卵只能培养出20%的健康后代。
李劲松还提到,该技术可以提供一种制造基因改造动物的有效方法,从而为实验室中对疾病的研究提供帮助。
伦理常规依然会受到挑战

尽管“人造精子”在医学方面的需求广泛,但关于“人造精子”研究,同时也引发了伦理的讨论。此次法国研究从男性精原细胞培育出精子细胞,看起来伦理问题还不太大。夏志表示,“但是,如果偷偷取得某人精原细胞,不需要偷精或是正常性生活,便可无声无息的将之受精,培育出一大堆的后代。这时安全性、伦理常规也会受到挑战。”
目前,与法国这项研究技术不同的是,国外相关的研究提到,在实验室环境下干细胞可以被培育成精子细胞。全球各个不同实验室将干细胞转分化培育成精子细胞,技术不尽相同,有的是用精卵作用,有的是用化合物或小分子,有的是用新的基因编辑技术。
2014年12月24日,发表在《细胞》杂志上的一项研究中,科学家不仅首次将皮肤细胞完全在体外诱导成为诱导干细胞(iPS),并使其分化成人类原始生殖细胞(hPGCLC),助力构建出人类精子和卵子的第一步。
中国科学院遗传发育所高级工程师姜韬就此技术表示,卡利公司是将原生殖细胞进行体外培养,与2014年发表的皮肤体细胞分化成原始生殖细胞对比有很大的区别。在伦理上首先就有很大的不同,此次是将生殖细胞进行体外培养,获取方式、培养过程、人工授精过程都符合国际公约,“说白了,就是将人工授精技术进行了阶段性的前移,让那些并不能产生精子的男性具有了孕育自己下一代的可能,因为提取的精原细胞就是精子的前身,可以说这项技术就是将试管婴儿技术进行了完善”。
此外,姜韬还补充了一点:将生殖干细胞进行体外培养进而使患者受孕,这是技术上的进步,但是还应考虑到在受孕之后会不会将不孕的基因也传递给下一代,如果下一代仍保留了这个基因,那么整个族群就会一直需要靠技术的支持而繁衍,“这就需要从人道主义关怀的大角度再进行思考,是否需要基因编辑技术的介入,将不孕的基因进行敲除?基因编辑技术本身能否实现这一期望,这都要靠科技力量去实现,且仍待从伦理的角度进行探讨”。
或许,随着科学技术的进步,不需要男人,甚至连女人也不要,生孩子都是可能的事情。其实,最可怕的是,若某天真的完全可以把皮肤细胞转分化为生殖细胞,那就麻烦了,会出现很多伦理道德问题。可以想象,如果到那时候,比如女方喜欢某个人,不需要跟男方发生性关系,只用弄到男方的皮肤细胞(非常易得),就可以给他生孩子了。“当然,这点在国际上已经有公约,任何有悖伦理的生殖技术都不可用于人类胚胎的改造,所以不需要男人的生育在现阶段仍不被允许”姜韬补充道。
目前,还令人疑惑的是,未来通过人工培育的精子质量和普通男性自然生成的精子会完全一样吗?夏志解释,“人工的跟自然的是不一样的,除非我们将其百分百的研究清楚。人工模拟自然物,自然过程是人类探索世界,进行科学研究的必然过程。相信随着我们研究的不断深入,人工精子质量会无限类似自然生产出的精子,甚至某种角度来看更好。”
澳学者称500万年后男性或将从地球完全消失
澳大利亚专家预测称,500万年后地球上的男性或将完全消失,地球将恢复母权制。

澳大利亚学者珍妮格拉夫和她的研究小组认为,男性的Y染色体在近几年大幅减弱。专家举例称,如果此前Y染色体携带约1000个基因,那么现在Y染色体携带的基因数量已减少约一半。与此同时,X染色体并没有太大变化。值得注意的是,如今生女孩已经比生男孩更常见。
学者还指出,至男性完全从地球上消失还有大约500万年,在此之前希望专家们能找到解决该问题的有效方法。(编译:乔京晶)

















