首次!三篇中国原创研究同时登上《神经元》
 |
|
图1.2017年12月20日出版的《神经元》封面为北京师范大学李武研究团队工作。 |
一次刊发三篇来自中国科学家的文章,封面也来自其中一篇,这是2017年12月20日出版的最新一期神经科学期刊《神经元》(Neuron)。
这三篇文章涉及视觉信息处理的机制和过程、钙离子非依赖性神经分泌形式等前沿问题。
最新上线的一篇是北京师范大学教授章晓辉团队关于两类中间神经元在视觉信息处理的相互作用的研究。
视觉是哺乳动物感知外界信息的非常重要的途径。之前大量研究表明,对视觉刺激信息的处理依赖于初级视觉皮层神经元集群协同完成的。局部场电位(local field potential, LFP)反映了神经元网络局部神经元集群活动状态,比如,LFP中的β波和γ波的振动对于视觉的注意力以及特点获取都很重要。之前的研究表明,GABA能中间神经元在产生以及调控神经元振动中起到重要作用,但是不同亚型的中间神经元是如何相互协作调控特定的波长活动,目前还不清楚。
表达生长素抑制素(somatostatin,SOM)和小清蛋白(parvalbumin,PV)的神经元是两种抑制性中间神经元。在这篇文章中,章晓辉团队通过光遗传技术,对小鼠的初级视觉皮层中的这两类神经元进行研究,发现SOM和PV中间神经元分别与大脑皮层的β波振动和γ波振动的产生及调控相关。
 |
|
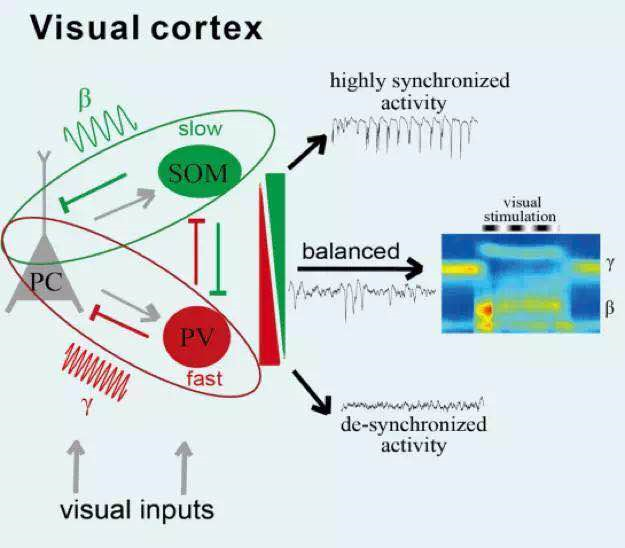
图2.SOM和PV中间神经元分别与大脑皮层的β波振动和γ波振动的产生及调控相关(来源:Chen et al., Neuron, 2017)
|
当抑制SOM细胞放电时,会减少自发的低频波振动,同时也会有选择性的减少视觉导致的β波振动的提升,这些研究结果暗示了SOM细胞在维持低频波的振动上起到了重要作用。当抑制PV
细胞活动时,会提高宽频范围的同步自发活动,阻止视觉刺激导致的β波和γ波振动变化,这些研究成果暗示了PV细胞防止神经元在宽频范围内高强度共振,进而在视觉介导的β波和γ波振动中起到了稳定作用,使得兴奋和抑制处在平衡状态。
由于β波和γ波振动在皮层中的出现还依赖于感觉的输入以及更高级的皮层调控,因此本次研究的发现或许为理解从下到上和从上到下的信号互作控制皮层动态提供了一个环路基础。总的来说,本次研究为皮层中β波和γ波振动的产生以及调控机制提供了更加具体的细胞学机制。
封面文章则为北京师范大学教授李武研究团队的工作,关于不同视觉皮层如何协调合作从复杂的视觉背景中提取出物体的轮廓,12月7日在线发表。
动物为什么能够在密林中发现捕食者的身影?通常认为,识别物体的轮廓,视觉信息需要在不同的视觉脑区被一步步地解码,最终由在高级视觉脑区(V4)的神经元整合这些解码而得到。通过同时记录猕猴的初级(V1)和次级视皮层(V2),李武研究团队发现,当高级视觉脑区识别出轮廓信息后,会回过头来调节初级视皮层的活动:经由V2的中层细胞到达V1的表层和深层细胞。研究者进一步发现,这一反馈信号在视觉背景中有很多干扰的时候尤为强烈,从而解释了为何视觉系统特别善于从繁复的背景中发现和关注被隐藏的轮廓。
北京大学分子医学研究所教授周专带领的团队的工作则于11月30日在线发表,他们首次在在哺乳动物的背根神经节(DRG)中,揭示了一种由钙离子通道Cav2.2介导的钙离子非依赖性神经分泌形式。
 |
|
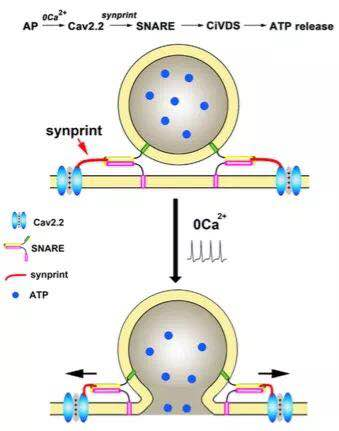
图3.钙离子通道Cav2.2介导的钙离子非依赖性神经分泌模型机制。(来源:Chai et al., Neuron 2017.) |
在经典的神经分泌模型中,动作电位刺激位于突触的钙离子通道,导致钙离子内流,从而使囊泡膜与细胞质膜融合,完成钙离子浓度依赖性分泌(CDS)。背根神经节位于脊髓后根神经,是痛觉和触觉信号传入大脑的必经之路,而它的神经分泌也与大脑对这些信号的正确感知密不可分,其重要性不言而喻。研究人员发现,在位于背根神经节的神经细胞中,钙离子通道Cav2.2可以直接与SNARE蛋白复合体(一种帮助囊泡与细胞膜融合的蛋白复合体)结合。在受到动作电位刺激后,Cav2.2-SNARE复合体可以在没有钙离子的情况下,诱导囊泡与细胞膜融合,释放ATP。
《神经元》为细胞出版社旗下期刊,是神经科学领域的重要学术杂志。早在2011年,中科院上海神经科学研究所和南京大学生命科学学院的两位学者曾点评《神经元》在2010年9月至2011年3月连续刊登5篇中国学者研究论文的现象,认为这“表明我国神经科学的研究水平在某些领域内正在迅速提高并步入国际先进行列”,据了解,这是《神经元》第一次同时刊登三篇来自中国的原创研究。正如两位学者六年前所言,期待随着中国科研基金资助环境的逐渐改善和神经科学界的努力,今后有更多的来自中国的原创性研究论文。
参考文献:
1.Chen, Rujia, et al. "Synergistic Processing of Visual Contours across Cortical Layers in V1 and V2." Neuron (2017). DOI:10.1016/j.neuron.2017.11.004
2.Chai, Zuying, et al. "Ca V 2.2 Gates Calcium-Independent but Voltage-Dependent Secretion in Mammalian Sensory Neurons." Neuron (2017).DOI: 10.1016/j.neuron.2017.10.028
3.Chen, Guang, et al. "Distinct Inhibitory Circuits Orchestrate Cortical beta and gamma Band Oscillations." Neuron(2017). DOI: 10.1016/j.neuron.2017.11.033
4.顾一希&王雨轩. "最近《 神经元》 杂志连续刊载我国学者原创性研究成果." 生理通讯 30.

















