���죬����һ�ڡ���ѧ����־���ߣ���������Ⱥ�방֢���ٵǷ��档����ѧ����־�ı༭���ò�ͬ�ij�����Ⱥƴ���ˡ���֢�д�����ģ������ǿ����Щ����������������Ʒ�����Ҫ�ԡ�

������һ�ڡ���ѧ����־�ķ��棨ͼƬ��Դ��V. Altounian / Science��
�ڱ��ڡ���ѧ����־�У���ƪ�ذ��о�ͬ�ڷ����������еı����������⳦����Ⱥ�Ļ������Ÿ��õ�Ԥ���е���ָ��ȱ��������Ⱥ���������Ʒ�����Ч����ˣ���������ĵ���������Ϊ���������Ʒ�����Ҫ��ɲ��֣�
��һ���о����������������ڵĿ����顣Guido Kroemer������Laurence Zitvogel���ڵ��Ŷӷ��֣�������Ⱥ�������Ʒ���Ч�����˹ؼ����á�������ʹ�ÿ����غ�PD-1�Ʒ���Ч���ͱ�úܲͨ���Էΰ����������ߵ�ȡ���������о���Ա�Ƿ�����Щ���������Ʒ�������Ļ��ߣ�����ȱ��һ�ֽ���Akkermansia muciniphila��ϸ�������������С��ʵ��֤��������ϸ�����洦�����ȣ��������÷����ֲ�ķ������ֱ����ÿ����ش�������С�����������Ʒ���Ӧ��������ֲ���ˡ������Ʒ��з�Ӧ���͡������Ʒ���Ӧ���Ļ��ߵľ�Ⱥ����ͬ�о���ԱԤ�ڵ�������ǰ�ָ��˶������Ʒ���Ӧ�𣬶����������ɶ������Ʒ�û��Ӧ������Ȥ���ǣ������ú����ٿڷ�Akkermansia muciniphila���������������Ʒ�����Ч�������о������֧���˳�����Ⱥ���ڿ�PD-1�����Ʒ�����Ҫ�ԡ�
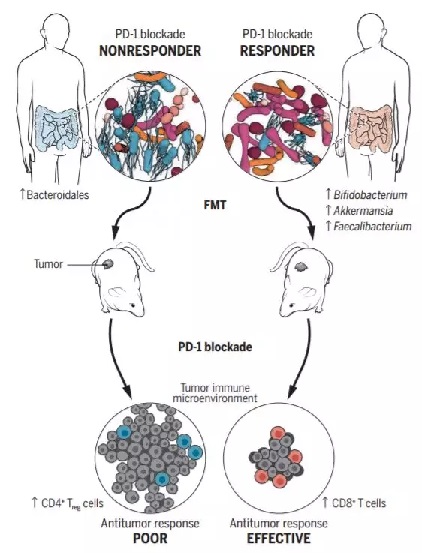
���в�ͬ�����С�����������Ʒ��ķ�Ӧ��Ȼ��ͬ��ͼƬ��Դ������ѧ����
���ڡ���ѧ����־�ϵ�������ƪ����������ע��ɫ��������Ҳ�Ƕ�PD-1�����Ʒ������������Ӧ֢�����У�һ���о��ĸ�������MD����ɭ��֢���ĵ�J. A. Wargo���ڣ���һ���о�������֥�Ӹ��ѧ��Thomas F. Gajewski�����Ŷӡ�
ǰһ���о���о���Ա������112�����ܿ�PD-1�����Ʒ��Ļ��ߵĿ�ǻ�볦����Ⱥ�����Ƿ��֣���Щ�������Ʒ����з�Ӧ���Ļ��ߣ����Ⱥ����ɺͶ����Ծ��͡���Ӧ���Ļ�����������ͬ����30�����з�Ӧ���Լ�13������Ӧ���Ļ��߷��������������ǰ������Ruminococcaceae�����ϸ����ȸ��ߡ��������Եķ������һ�����֣�ǰ�����ڵĺϳɴ�лͨ·��Ϊ�ḻ��ϵͳ�������뿹����������Ҳ��ǿ��
��һ���о��������Ƶ���ơ���ת���Ժ�ɫ�������߽��������Ʒ�ǰ���о���Ա�Ǽ�������ǵķ����Ʒ������16S������RNA�������������Լ�����PCR�ļ��������ض���������˷��������Ƿ��֣���Щ���з�Ӧ���Ļ������ڣ� Bifidobacterium longum��Collinsella aerofaciens���Լ�Enterococcus faecium����Ϊ�ḻ������������Щϸ����С����������Ÿ��õĿ��ƣ�Tϸ����Ӧ��ǿ�������Ʒ���Ч��Ҳ���á�
��������Ϊ��һ�����Ʒ��𣿣�ͼƬ��Դ������ѧ����
����ѧ����־ͬ�ڿ����˷�������ѧChristian Jobin���ڵ�ר����������Ϊʹ�������飬������������ȫ�µľ��Ʒ�������Jobin�������ԣ���������Ѱ����һ����ҩ�ı��⡣��ͨ�������������Ʒ�֮��ĵ�·����Ϊ���Ǵ���ȫ�¶�����
�ο����ϣ�
[1] Gut microbiome modulates response to anti�CPD-1 immunotherapy in melanoma patients
[2] The commensal microbiome is associated with anti�CPD-1 efficacy in metastatic melanoma patients
[3] Gut microbiome influences efficacy of PD-1�Cbased immunotherapy against epithelial tumors
[4] Precision medicine using microbiota

















