基于数目高达524万居住于英国人士的匿名医疗记录的研究
随着公众的腰围不断膨胀、健康栏目的头条新闻中总是少不了肥胖这一话题、这次当然也不例外。
更重要的是、此番发表于权威期刊《柳叶刀》上的研究分析了体重指数BMI和22种最常见的癌症之间的风险关联、而且进一步强化了相应的证据。
基于多年研究、研究人员已经十分确信有7种癌症在超重或肥胖人群中更为常见:食管癌、肠癌、胰腺癌、胆囊癌、乳腺癌、肾癌和子宫癌。然而这次的新研究以前所未有的超大规模和严谨将更多种类癌症补充进了这张表单。
诚然、肥胖何以与那么多癌症之间有关联这一点认识得还不充分、但是新的发现再次强化了一个既有观点:超重或肥胖肯定会增加罹患癌症的风险。
此项研究的团队隶属于伦敦卫生与热带医学学院(London School of Hygiene & Tropical Medicine)、梳理了数目高达524万的英国居住人士的匿名医疗记录、其中含有医生留下的身高与体重记录。于是每个人的BMI就能被计算出来。

BMI改变、癌症风险怎么变?
接下来团队开始观察BMI与癌症之间的关联。研究规模极为庞大、所分析的数据较此前任何研究都要多得多。然而这一点却是至关重要的――因为通过这样给出的证据才更加强有力。第一轮研究中、BMI就和17种癌症扯上了关系、较此前所认为的已经多出了10种。不过真正引人入胜的却是研究随着BMI上升、癌症风险将会发生如何的变化。这就涉及每一种癌症类型的具体分析了。
譬如、分析结果表明:『肥胖是女性子宫癌的最大风险』。女性的BMI越高、则日后罹患子宫癌的概率就越高。同样地、胆囊癌、肾癌和肝癌也和肥胖之间存在实质性的关联、其他还有结肠癌、宫颈癌、甲状腺癌、卵巢癌、绝经后乳腺癌以及白血病。
研究团队并未仅仅观察高BMI时的情形。他们还发现、体重不足时口腔癌、胃癌和肺癌的风险会升高。不过这一现象也可能是由于吸烟造成的、因为不吸烟人群中未发现这种效应、而且这几种癌症原本就是和吸烟高度相关的类型。
此外还发现性别也是一个因素。譬如同样超重时男性罹患肝癌的风险要比女性来得高。
总体而言研究团队发现了一种【最适效应】(Goldilocks Effect)――即有些癌症更偏好超重人群、而有些则多发于体重不足的人群。换言之就是、在预防癌症方面最理想的状态应该是『不太胖、不太瘦、刚刚好』。
不过、当研究者们仔细观察BMI升高对于不同类型癌症风险变化的影响时、情况就变得扑朔迷离了。
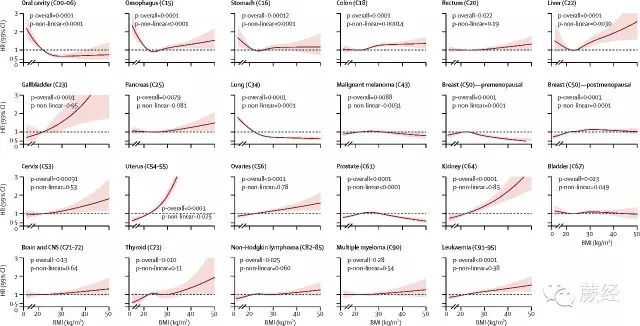
癌症与BMI之间关系的清单↑
癌症风险与BMI之间的关系非常复杂
对于某些癌症而言、癌症风险会随着BMI升高而渐渐增加、即所谓的线性关系。但也有一些癌症风险的变化方式却难以预知。因此此项研究的最终结果表明BMI和癌症之间的关系是极为复杂的、其意义更多是为今后的研究撑起肩膀、而并非给到一个确切的答案。
同时这项研究还提示了一点:即便通过如此超大规模的数据分析依然无法确切了解癌症与BMI之间到底是怎样的关联――因为风险的变化形式很复杂、并没有相同的模式可遵循。
譬如:
BMI本身是否衡量肥胖程度的最佳标准?很有可能不是。虽然BMI是目前最好的通用测量标准、但是BMI是不是最精确的测量标准呢?不好说。实际上这项研究的主要局限是在于没有备选的肥胖测量手段(例如体脂百分比数据)。
锻炼扮演怎样的角色?体育锻炼可能有助于减少许多癌症的风险、但没有进行衡量。这是这项研究的另一短板。
而最重要的一点或许是、依然没有真正搞清楚:『减重到底是否有益于降低癌症风险』。为此我们需要极为详尽的数据和长时间的跟踪、而现阶段能够说的只有一个:【保持健康体重至关重要】。
当然、即便存在上述不完美之处、这项研究的超大规模以及统计严谨性依然使之成为了迄今为止最为综合的肥胖-癌症关联研究。

那么对于一般公众而言其意义何在?
肥胖是癌症的重要危险因素之一。这项研究估计英国每年有12000例癌症的发生与体重问题有关(虽然之前的研究认为的数字更高、达17000例)。而且肥胖还不仅仅于癌症有关。其他很多疾病、如糖尿病和心脏病等都与肥胖有着千丝万缕的关系。有关肥胖危害的证据越来越多、将促使英国在国家层面上将这一话题上升到政策讨论的高度。
最后值得一提的是、这项新研究还提示了匿名数据在医学研究领域的重要作用。可供研究分析的数据越多、癌症风险的变化模式与原因就会表现得越清晰、最终帮助人们找到如何将风险最小化的方法。
参考:
Body-mass index and risk of 22 specific cancers:a population-based cohort study of 5・24 million UK adults
http://www.thelancet.com/journals/lancet/article/PIIS0140-6736(14)60892-8/fulltext
http://scienceblog.cancerresearchuk.org/2014/08/13/obesity-and-cancer-adding-more-weight-to-the-evidence/?utm_source=twitter_cr_uk&utm_medium=cruksocialmedia&utm_campaign=owntwitter_tweet
肥胖致癌!神药阿司匹林或可抑制肥胖相关性癌症发生!

最近的研究表明,新出现的转化细胞通常通过与周围正常上皮细胞竞争从而在上皮组织中被消除。 这种癌症预防现象被称为上皮性抗癌(EDAC)。 然而,关于EDAC在致癌过程中是否减少以及如何减少,目前尚不清楚。在本研究中,研究人员发现高脂饮食(HFD)可显着减弱转化细胞的消除频率。 该过程涉及脂质代谢和慢性炎症。肥胖可以显著影响正常细胞和转化细胞之间的竞争性作用,进而产生致癌作用。 惊喜地是,阿司匹林可显着促进上皮组织清除转化的细胞。 这么说来,万能神药阿司匹林又有新的用途了!

在癌发生的最初阶段,转化发生在上皮层内的单个细胞中。新产生的转化细胞和周围的正常上皮细胞经常为了生存而相互竞争,这种现象称为细胞竞争。例如,当RasV12转化细胞被正常的上皮细胞包围时,RasV12细胞会从上皮顶部被消除。这些数据暗示了正常上皮细胞具有不涉及免疫细胞的抗肿瘤活性,这个过程被称为上皮性抗癌防御(EDAC)。然而,肥胖,衰老和感染等环境因素是否影响EDAC仍然未知。
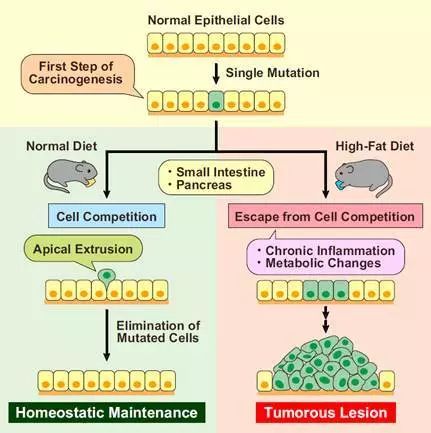
该试验的实验过程
肥胖是影响EDAC的主要危险因素之一。肥胖可以诱发各种全身性疾病,例如脂代谢改变,激素分泌失调,生态失调和慢性炎症。显而易见的是,肥胖个体具有某些类型的恶性肿瘤更高的发生率,包括结肠癌,胰腺癌和乳腺癌。先前的研究揭示了肥胖如何促进肿瘤生长和恶性进展的分子机制,如氧化应激,慢性炎症,生态失调和激素改变。然而,肥胖是否以及如何参与肿瘤发生尚不明确。
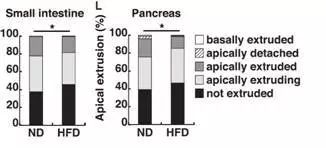
在小肠与胰腺中的转化细胞清除率
研究人员发现减少高脂饮食可增强肠道和胰腺上皮细胞消除新出现转化细胞的能力,但并不能减少肺部的转化细胞。这一结果似乎与肥胖和肠道及胰腺癌症的发生存在相关性。该研究还表明,慢性炎症部分参与肥胖引起的EDAC抑制。慢性炎症涉及各种细胞的募集和活化,包括免疫细胞和成纤维细胞。这些细胞分泌的可溶性因子可能影响正常细胞和转化上皮细胞之间的竞争性作用。慢性炎症如何影响细胞竞争的分子机制需要在未来的研究中阐明。
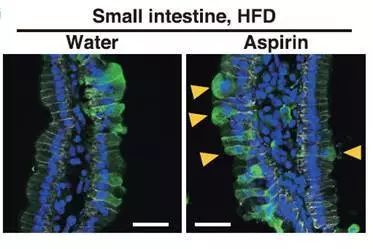
阿司匹林可拮抗肥胖致癌作用
同时,在这项研究中,研究人员证明阿司匹林可以增强高脂饮食小鼠体内转化细胞的清除率,这意味着强化EDAC可以成为非甾体类抗炎药在癌症预防中的潜在靶标之一。这些研究的进一步发展将加强在生理学和病理学层面对细胞竞争的全面理解。
参考文献
Ayana Sasaki, Takahiro Nagatake,Riku Egami. Obesity Suppresses Cell-Competition-Mediated Apical Elimination of RasV12-Transformed Cells from Epithelial Tissues.

















