8月28日,中国大陆首个免疫检查点抑制剂纳武利尤单抗注射液(nivolumab)终于与广大患者见面了。
话说起来,肿瘤免疫治疗的概念兴起好像也就是这几年的事儿,诸多企业在争抢的免疫检查点(PD-1/PD-L1)抑制剂、热议的CAR-T疗法,这才让大众把视线聚焦到这种潜力无限的“新兴”疗法上。
其实不然,在癌症的治疗史上,免疫治疗已经有百年以上的沉淀,实际上它才是第一个非手术的癌症疗法。
胆大的年轻人
1890年,一位名叫Elizabeth Dashiell的17岁少女,在夏季旅行中不小心弄伤了手臂。没过几周,她受伤的手开始肿胀而且疼痛难忍,于是她来到医院求诊。
为她看诊的医生名为William Coley。这位Coley医生年轻得很,1888年才从耶鲁大学本科毕业,之后就在哈佛医学院学习,同时在医院做实习外科医生,1890年他才刚刚开始在纽约癌症医院独立执业。也就是说,Elizabeth可以算是Coley真正意义上的第一批患者。
哦对了,纽约癌症医院,几经变迁,就是后来的纪念斯隆・凯特琳癌症中心(MSKCC)[2]。为了说起来方便,咱们下文就统称MSKCC吧。

17岁的Elizabeth,左边是她的友人Jhon D. Rockfeller Jr.,这个帅哥后来又给MSKCC捐地又是出资,对癌症研究进展的贡献不比科学家小
像Elizabeth这种肿胀疼痛的症状,看起来很像是外伤感染了,于是Coley给她做了个组织检查。检查结果令人伤心,Elizabeth的手臂并非感染,而是患上了软组织肉瘤,而且肿瘤已经侵袭到骨骼了。
在那个放疗化疗什么疗都没出现的年代,这就是绝症,除了手术截肢毫无办法。Coley截掉了Elizabeth的右前臂试图阻止癌症扩散,然而无力回天,一个月之内,肿瘤就扩散到肺部、肝脏和其他位置。1891年1月23日,Coley眼睁睁看着这个花季少女在痛苦中死去。

William Coley(1862-1936)
对于一个初出茅庐的医生来说,亲眼看着病人悲惨死去不可谓打击不大。这也让Coley坚定了寻找新肉瘤疗法的决心。既然对癌症的研究还很初级,那么就从故纸堆里翻资料!他找出了过去15年份的医院病例档案,想看看其他医生是怎么处理肉瘤的。
别说,还真给他发现了一些有意思的东西。
有一个名叫Fred Stein的德国肉瘤患者,他的肿瘤长在脖子上,很难通过手术处理,本来医生们都已经放弃了,让他该吃吃该喝喝准备后事了。可是在他偶然得了丹毒,也就是现在我们所说的化脓链球菌感染之后,肿瘤居然逐渐消失了!

丹毒
这事儿已经过去七年了,也不知道这位患者后来怎么样了。Coley立刻从医生化身大侦探,他来到当时德国人普遍居住的纽约市曼哈顿下东区,挨家挨户敲门寻找这个脖子上应该有疤的Stein,最后还居然还真的找到了――活的,健康的,没癌症的。
除了Stein,Coley还找到了47例类似的病例,而且查找以前的文献资料,他还发现,在1853年和1866年,都曾经有学者发现类似的感染令患者肿瘤消退的病例[5,6]。
这么多的相似病例,让Coley有了一个相当大胆的想法:如果感染能令肿瘤消退,我们是不是可以故意制造感染来治疗癌症呢?

链球菌
这个胆大的年轻人真的是敢想敢干。考虑到丹毒是很容易致命的,Coley下面的行为简直就像是“草菅人命”了,他竟然直接给患者注射活的化脓链球菌!
不得不说Coley这个时候运气还是蛮不错的。首个试验对象是个病得无可救药的意大利人Zola,他的肉瘤长在喉咙里,别说吃饭了,呼吸都困难。在不同剂量反复注射中,Zola终于患上了致命的感染,但是同时,他的肿瘤在24小时之内就开始缩小。
Zola完全康复了。

Zola
在这之后的两年里,Coley又用类似的方法治好了十多名患者。为了更安全,还改进了配方,使用了灭活的链球菌和沙门氏菌诱导感染,也就是“Coley毒素”。
但是,Coley毒素是怎么治好患者的呢?Coley自己也不太明白。十九世纪九十年代,科学家尚且刚刚开始接触免疫这个概念,从原理上就谁都说不清楚;Coley在治疗的时候,为了引发一定的感染又不至于杀死患者,注射细菌的剂量和次数都是随用随调的,效果也不确定,看起来就不像是很科学的治疗方法;更何况,Coley还真的治死了两个人呢。
所以1893年,Coley公布研究成果的时候,学界都是抱着看“祖传老偏方”的姿态去怀疑他的,美国癌症协会毫不客气地质疑道,“我们还需要更多的研究来确定这种疗法对癌症患者的可能益处,如果有的话。”
还没等Coley证明自己,1901年,放射治疗出现了。放疗可是能够切切实实令癌症患者好转的,所以科学家们一窝蜂地跑去搞放疗了。

1915年用于治疗面部上皮瘤的放疗设备
当时批判Coley毒素最厉害的一个人叫James Ewing[8],就是尤文氏肉瘤的发现者,他也是放疗的坚实拥趸。1910年,他来到MSKCC,在他手中,MSKCC成为头部医学机构,放疗也得已发扬光大。
不过想必在Ewing手下工作的Coley,晚年并不好过吧。Ewing执掌大权期间,整个MSKCC都不允许使用Coley毒素,他主持建立的癌症登记系统甚至拒绝登记Coley的病人,因为按照他们的思路,能够被Coley毒素治愈的患者,绝对是误诊了。直到1936年Coley去世,Coley毒素也没有获得学界的认可。

James Ewing(1866-1943)
他是尤文氏肉瘤的发现者,也可以说是那个时代最伟大的癌症医生之一。只可惜学术上观点的不同让他忽视了Coley的发现。
三个Coley
一个Coley倒下去,两个Coley站起来。Coley身后还有一双儿女,他们以不同的方式继承了父亲的遗志。
Coley的儿子Bradley也在MSKCC工作,他继续了Coley毒素治疗的临床研究。二十世纪四五十年代,Bradley用老爹留下的方案治愈了不少患者,有的患者直到今天还活着。

Donald Foley在13岁时被诊断为肉瘤,是Coley毒素让他免于失去一条手臂,并顺利地长大,成为了一名职业消防员。他今年78岁。
然而Bradley的故事简直像是Coley的翻版。二战期间,美国开展了化学武器计划,计划中一个科学家叫做Cornelius Rhoads[9],是他发现芥子气具有治疗癌症的潜力,他也主持了后来第一种化疗药物氮芥的研究[10]。化疗和放疗一样,疗效强大而且可预测、可以标准化,所以那时科学家们又都跑去搞化疗了。
Rhoads在1939年掌管了MSKCC的研究大权。你说巧不巧,Bradley和老爹命运真是一样一样的,默默工作没人重视,等到他退休,Coley毒素再也没人搞了,彻底被锁进了档案柜。

Bradley Coley
Coley的女儿Helen倒并不是个医生,甚至也不懂生命科学。她在整理父亲的遗留手稿时发现,Coley这一辈子用Coley毒素治愈的患者怕不是有近千名!这么多的成功案例,如果全用误诊来解释也太牵强了,这里面一定还有更多值得探究的科学原理!
这个姑娘是真的刚,她拿着整理好的父亲的科研资料,直接找到当时各位大牛的办公室去,不厌其烦地推广Coley毒素。先不说她一个门外汉又是女性、在当时要受到多少歧视,就看那个年代,二十世纪三、四十年代,学界被放疗统治,说话最算数的James Ewing是Coley最大的学术敌人;没过几年,化疗时代到来,当时的掌门人Cornelius Rhoads也对Coley毒素毫无兴趣,把Helen拒之门外。

抱着Helen读书的Coley
要不说这个姑娘刚呢,1953年,她拿着两千美元赞助款,在朋友的帮助下成立了非营利组织癌症研究所(CRI),专注细菌毒素和癌症免疫学研究,希冀有一天能够证实父亲的理论是正确的。
最奇迹的是,CRI确实做到了,而且近代免疫学历史上,几乎每一个重大的发现都和这个默默无名的机构有关。
现在打开CRI的官方网站,我们看到的就是下面的界面,显眼的位置上写着,“All cancers can be potentially be treated with immunotherapy(所有癌症都可能用免疫疗法治疗)。”

另一个优秀的年轻人
在CRI成立最初那段日子里,Helen过得很艰难。
1953年,学界对免疫系统的认识还是很零散的,科学家刚刚对抗原抗体反应摸到一点苗头,但对免疫细胞还是一无所知,T细胞此时连名字都没有。Helen拿着时刻会用光的赞助,招募研究者,一边开展临床试验,一边进行基础研究。
不过问题还是那个问题,用Coley毒素治疗癌症患者,依旧是个没法量化也说不出道理的方案。
让事情变得更糟糕的是,1965年,美国癌症协会把Coley毒素列入了“未经证实的癌症治疗方法”,这等同于官方盖章,说CRI进行的工作是在骗人。
事情的转机出现在二十世纪六十年代末尾,Helen遇到了Lloyd Old。

Lloyd Old(1933-2011)
Old这个人可以说是很优秀了。他1958年来到MSKCC开始自己的学术生涯,1959年就搞出了卡介苗(BCG),论文登在《自然》杂志上[13]。卡介苗主要由减活的结核杆菌构成,Old发现,注射了卡介苗的实验动物对肿瘤生长有更强的抵抗力。
看,这个东西是不是和Coley毒素有点像!
那就难怪Old和Helen一见如故、引为至交了。Helen被Old强大的学术能力所折服,Old也对Helen的执着信念印象深刻。在此后的几十年里,他们两人就是科研路上的最佳拍档。

两个人晚年还经常在一起讨论学术
Old在学术上颇有成就,除了卡介苗,他又陆续发现了主要组织相容性复合体(MHC)和白血病的联系,发现了我们今天用来区分T细胞种类的CD8表面抗原,发现了EBV病毒与鼻咽癌的关系,发现了关键的免疫分子肿瘤坏死因子(TNF),他是p53蛋白的发现者之一,在肿瘤抗原研究上更是成就无数……今天我们把他称作“现代肿瘤免疫学之父”,Old当之无愧。
有了这样一位备受尊重的科学家的支持,Helen的工作顺利了很多,癌症免疫学的发展逐渐步入正轨,越来越多的年轻学者投入了这个领域,并在接下来的几十年里拿出了耀眼的成绩。
用一句现在流行的话来说,他们改变了潮水的方向。
这也是和前辈学者的悉心教导有关的。Old这一辈子手把手带出了无数癌症免疫学领域内的头部学者,他的学生中,有一个人叫做Jedd Wolchok。

Jedd Wolchok
PD-1 ! PD-1 !
Jedd Wolchok这个名字,说起来大家可能不是很熟悉,但是提到他的好伙伴James Allison教授,那么了解免疫检查点抑制剂历史的朋友们可能就要发出恍然大悟的“哦~”了。
1996年,Allison在《科学》杂志上发表了一篇论文,他们首次证实,用抗体阻断T细胞表面CTLA-4受体的作用能够治疗小鼠体内的肿瘤[15]。Allison把这个治疗思路叫做免疫检查点阻断。

Allison和他的妻子,两人也是学术路上一对神仙眷侣
当时,人们普遍认为CTLA-4只是T细胞表面的一种免疫功能调节蛋白――很普通,和其他很多种蛋白一样――CTLA-4属于T细胞自我约束的一种机制,以免太强烈的免疫反应伤害到健康组织和细胞。
Allison的论文发表之后,好多人都觉得挺玄的,愿意和他一起搞商业化的医药公司也不多,谁能想到这会是癌症治疗巨变的开始呢。准确嗅到这丝气息的是Medarex。这家公司在1999年拿下了CTLA-4抗体的专利,2000年就让世界见识到了免疫治疗的临床潜力。
2009年,Medarex被百时美施贵宝(BMS)收购,肿瘤免疫(I-O)药物研发从此进入了开挂的快速期。
2011年,CTLA-4抗体终于有了一个响当当的大名Yervoy(ipilimumab),而让它通过FDA严格审批的临床试验,正是Jedd Wolchok主持的。包括CTLA-4抑制剂和PD-1抑制剂联用在内,Wolchok至今还在积极探索让免疫治疗更好的方法。
ipilimumab诞生之后,学界才真的意识到免疫检查点抑制剂的威力,开始寻找CTAL-4之外的其他可用靶点。下面就该是PD-1的故事了。从1992年发现PD-1蛋白,到PD-1抗体走入临床,这期间的诸多波澜我们已经专门写了一篇文章来介绍,这里就不再赘述了。
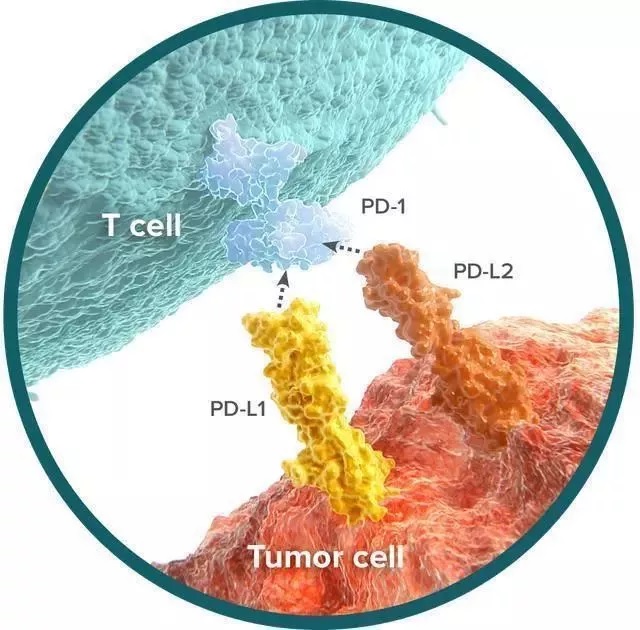
PD-1的机制和CTLA-4略有不同,它的相应配体位于癌细胞上
2014年,Opdivo(nivolumab)在日本获批,成为全球首个获得监管机构批准的PD-1抑制剂,彪悍的传奇就此正式开始。
作为PD-1抑制剂家族的大哥,nivolumab做了个相当好的榜样。4年之内,在全球批准了17个适应症,涉及肺癌(NSCLC、SCLC)、黑色素瘤、肾癌、霍奇金淋巴瘤、头颈鳞癌、膀胱癌、结直肠癌、肝癌、胃癌在内的9个瘤种,是目前获批适应症最多的PD-1抑制剂。
2018年6月15日,nivolumab获中国国家药品监督管理局(NMPA)批准,成为第一个登陆中国大陆的免疫检查点抑制剂,也是截止目前唯一在中国大陆获批肺癌适应症的PD-1抑制剂。根据AACR2017年大会上报道的checkmate-003临床试验的数据,nivolumab把晚期非小肺癌患者的五年生存率从不足5%提升到16%。
尽管目前nivolumab只在中国大陆批准了非小细胞肺癌一项适应症,但从BMS公布的全球临床试验数据来看,肝癌、胃癌等中国高发癌种也非常值得期待,针对中国患者的多项相关三期临床研究也正在进行中。
1891年,Coley把第一管Coley毒素注入患者体内,这实际上是人类第一次创造出抗癌疫苗。
2018年,免疫检查点抑制剂登陆中国,想必国内癌症免疫治疗的大幕,就此拉开。

















