无声的世界是怎样的?奇点糕没有体验过,没法说自己能够与听障者感同身受,但我们可以有一个共同的认知,听觉对人类的生活相当重要,无法听见声音会关闭个体认知世界的一种方式,如果这发生在儿童身上,甚至会影响他们的大脑发育。
全世界有约2600万先天性听力障碍者,60%由基因突变导致。其中约2-8%为常染色体隐性遗传性耳聋9(DFNB9),问题出自编码耳畸蛋白的基因OTOF。如果未能尽早治疗,这些孩子们可能都无法学会说话。
但是自60年前人工耳蜗发明以来,我们还没有发现一种可靠的耳聋治疗方式。
今日,《柳叶刀》杂志发表了一项重磅研究,科学家们终于拿到了应对DFNB9的利器。在复旦大学附属眼耳鼻喉科医院进行的全球首个遗传性耳聋基因治疗试验取得了令人欣喜的成功,参与试验的6名1-6岁儿童,有5名有了显著的听力恢复,随访26周时在0.5-4kHz下进行听觉测试,平均听性脑干反应(ABR)阈值从超过95dB下降至最低45dB。
这是什么概念?类比一下,就是从摩托车呼啸而过都听不见,到可以正常听到办公室内的人说话。
推荐大家看看下面小朋友做听力测试的视频,听到小朋友对爸爸说我爱你、对妈妈说你声音有点大的时候,奇点糕都有点鼻子一酸,不敢想家长的心情该有多激动。
这项研究的通讯作者为复旦大学舒易来、李华伟、王武庆,哈佛大学陈正一、东南大学柴人杰

基因治疗原理说来简单,本项研究的特殊之处在于,OTOF基因大小超出了腺相关病毒(AAV)载体的承载量,所以研究中使用的是双AAV载体,通过毛细胞特异性启动子Myo15控制基因表达。试验中直接将AAV1-hOTOF注射至患者的内耳。
参加试验的6位小患者年龄1-6岁不等,可以看到他们的基线ABR阈值均超过95dB,处于完全听力丧失的状态。其中年龄相对较大的4位小患者植入了人工耳蜗。
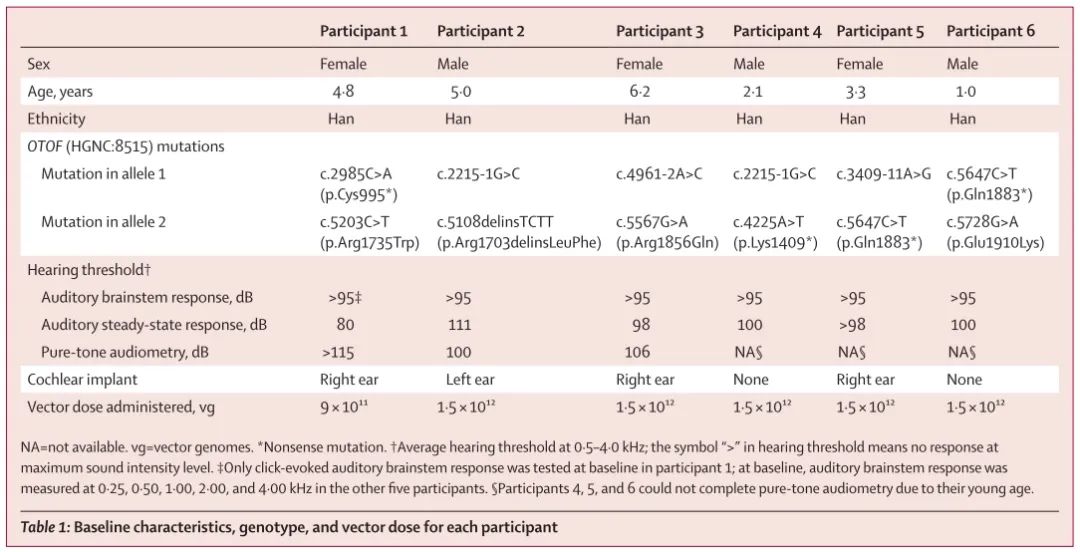
患者基线情况
研究采用了两种不同的注射剂量,9×1011 vg(30μl)和1.5×1012 vg(50μl),随访26周。
总的来说,AAV1-hOTOF安全性相当不错,除了5号患者出现了自发性的3级白细胞计数降低之外,其他96%的不良反应级别均较低。未观察到剂量限制性毒性。
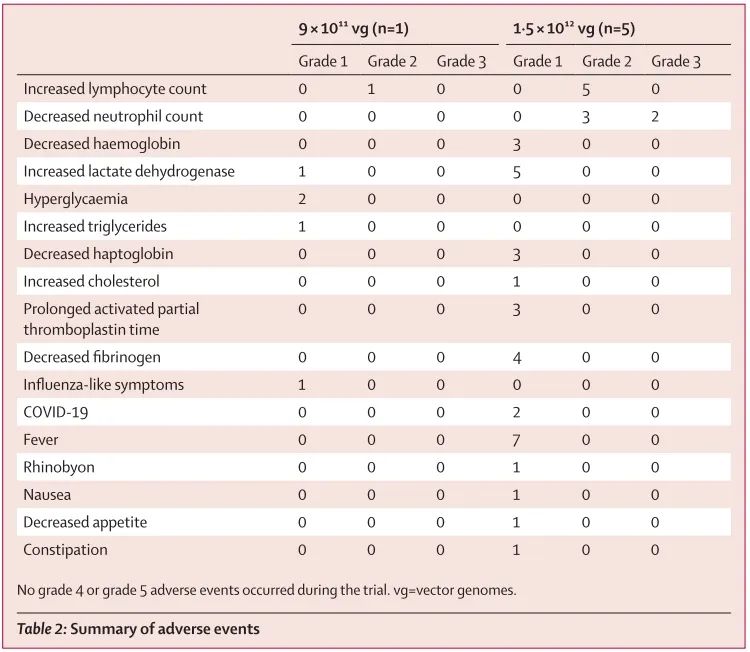
患者的不良反应
1号患者接受的是9×1011 vg剂量,基线ABR阈值>95dB,在试验第4/6/13/26周再次测试,ABR阈值分别为68/70/53/45dB。效果最好的一次测试,在0.25kHZ和2kHZ下,ABR阈值达到了35dB。
她的听觉稳态反应(ASSR)阈值在第4/6/13/26周分别为80/73/60/38dB,纯音听阈测试(PTA)阈值分别为71/68/55/30dB。
其余5名患者接受1.5×1012 vg剂量,其中2号患者未见听觉恢复。余下4名患者,在第26周ABR阈值分别达到48/38/40/55dB。
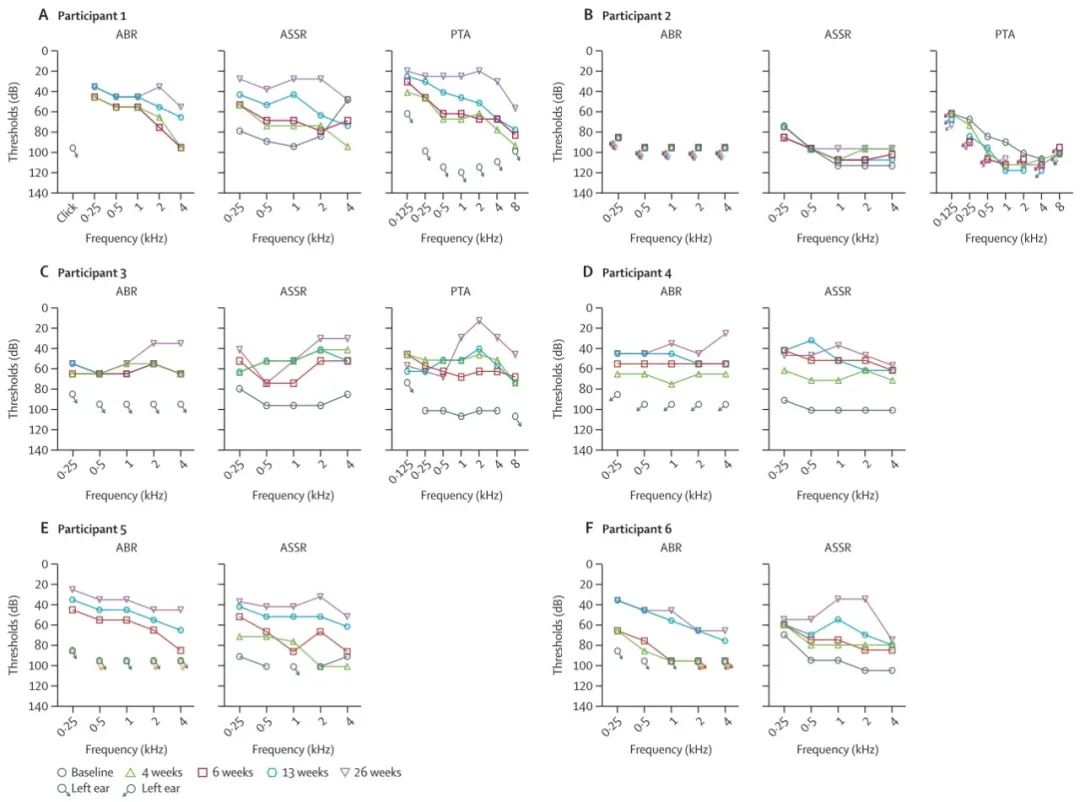
患者的ABR、ASSR和PTA阈值数据
未能改善听力的2号患者,基线AAV中和抗体水平较高,或许此前曾经感染过AAV,这些抗体中和了AAV1-hOTOF;也有可能AAV1-hOTOF从注射部位泄露,没能达到目标细胞。
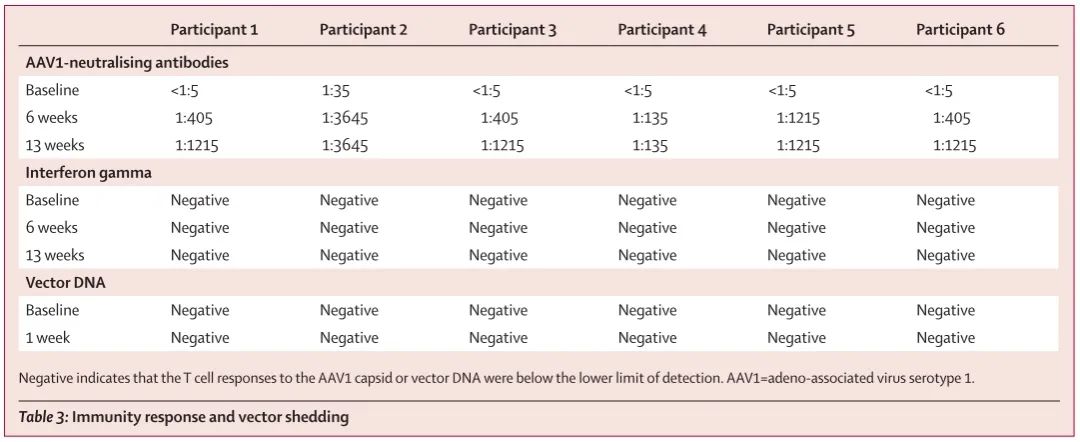
患者基线AVV抗体水平
这项研究是目前首个、也是迄今为止患者数最多、随访时间最长的遗传性耳聋基因疗法临床试验,AAV双载体应用的成功也给其他受限于基因大小的疗法提供了新路。

















