“永生难忘”的原因揭秘
2024-07-06,阅读:145
诺贝尔物理学奖得主、百岁老人杨振宁先生晚年回忆在清华的童年生活时曾说:“在我的记忆里,清华园是很漂亮的。我跟我的小学同学在园里到处游玩,几乎每一棵树我们都曾经爬过,每一棵草我们都曾经研究过。”凭借自己的记忆,杨先生依然可以清晰地想起半个多世纪前发生在童年时期的很多细节。
我们的记忆存储在脑内神经细胞突触中的一些分子中,如神经递质、蛋白激酶。神经细胞长出很多像章鱼的触手一样的东西,称为轴突或者树突。而突触是两个神经细胞进行信息传递的中转站,就像两根水管之间的接头。这些负责储存记忆的分子只能存在几个小时到几天之间。按照逻辑,它们消失的时候,我们的记忆也应该一起消失。但事实是,我们的记忆可以被保存数十年之久。理论和现实的矛盾,一直困扰着人们。
我们需要一个合理的解释。
上世纪科学家们提出了几种猜想,这些猜想可以分为两类:长期记忆被编码在DNA序列上(因为DNA不会在短时间内消失);或者每个突触上至少有一个大分子长期存在。然而从当时人类已了解的生物学知识来看,这两类猜想成立的可能性极低。
直到1984年,弗朗西斯·克里克(就是那位和詹姆斯·沃森一起发现DNA双螺旋结构并获得诺贝尔生理学或医学奖的科学家)提出了一种更合情理的猜想。“突触中的分子可以被新的材料取代,一次一个,而不会改变结构的整体状态,”克里克在《自然》杂志发表的观点文章中写道。他关于这种记忆的方式的猜想与希腊神话中的 “忒修斯之船”非常相似:将船上所有的旧木板替换成新木板后,这艘船依然存在。这艘船相当于我们的记忆,船上的每块木板可以看成是存储记忆的某种分子(可能是蛋白质或修饰蛋白质的酶)。
但猜想不等于事实,好奇心驱使我们向科学要答案。
今年6月发表在Science Advances上的一篇论文,给出了一个关于长期记忆合理的生物学解释。在这篇论文中,来自美国、加拿大和德国的研究者们发现KIBRA(kidney and brain expressed adaptor protein),一种蛋白质分子,在长期记忆中发挥关键作用。KIBRA和另一种称为蛋白激酶ζ(protein kinase Mzeta, PKMζ)结合在一起,共同维持旧的记忆。蛋白激酶ζ可以帮助持续增强突触的信息传导能力。
为了证明KIBRA-PKMζ结合体在维持记忆中的作用,研究者们把小鼠放在专门的环境下,学习如何躲避危险。小鼠产生躲避危险的记忆后一小时,研究者们向一部分小鼠大脑注射ζ-stat,一种阻止KIBRA和PKMζ结合的试剂。两天后,研究者们重新把它们放回原来的环境中。与没有接受注射的小鼠相比,这些被注射ζ-stat的小鼠失去了躲避危险的记忆。这说明,KIBRA-PKMζ结合体对维持长期记忆至关重要。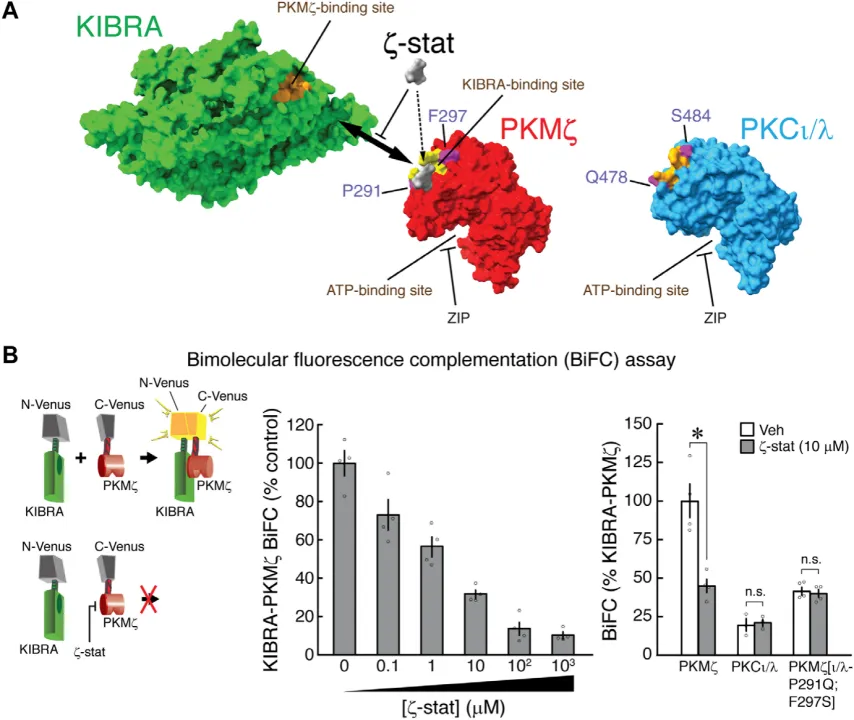
KIBRA(绿色)和PKMζ(红色)结合,以及ζ-stat(白色)阻止二者结合示意图。来源:https://www.science.org/doi/10.1126/sciadv.adl0030
但有没有可能,这些被注射ζ-stat的小鼠,永久丧失了记忆能力?为了排除这一点,研究者们把这些被注射ζ-stat的小鼠放到第二个场景中学习躲避危险,经过训练后,它们能记住如何在这个新的场景中躲避危险,但是它们躲避第一个危险场景的记忆依然没有恢复。这说明,小鼠的记忆能力并未消失。在长期记忆形成期间破坏KIBRA-PKMζ结合体,才会造成记忆的消散。
进一步研究后,研究者们发现,维持长期的记忆需要依靠KIBRA和PKMζ持续不断的相互作用。虽然KIBRA和PKMζ分子的寿命很短,大约只有几小时到几天,但是新的分子在源源不断地替换旧的分子,以确保KIBRA和PKMζ之间的相互作用不被中断。就像“铁打的营盘流水的兵”,只要“兵营”还在,一切就可以正常运转。而当ζ-stat打破了这种相互作用,长期记忆就消失了。
“我们发现的持久记忆的机制类似于新木板取代旧木板以长期维持忒修斯船。即使维持记忆的蛋白质被替换,也能让记忆持续多年。”Todd Sacktor说。Sacktor是美国纽约州立大学州南部医学中心的教授,也是这项研究的主要负责人之一。
生活中那些美好的瞬间值得我们一生回忆,但是一些过于痛苦的记忆却会不断消耗我们的精力,影响我们的工作和生活。在谈及这项研究成果的意义时,Todd Sacktor说道:“对我们如何保持记忆的深刻理解,将有助于指导我们未来阐明和解决与记忆有关的痛苦”。
一项科学上的重大突破,往往需要科学家们持之以恒地付出几十年的时间。从弗朗西斯·克里克提出“忒修斯之船”猜想,到科研研究证实这一猜想,已经过去整整40个年头。
这一发现对治疗阿尔茨海默病等记忆缺失相关的疾病也有重要意义。这类神经系统性疾病可能会干扰与记忆存储相关的蛋白质的相互作用。论文通讯作者之一、来自纽约大学朗格尼医学中心神经科学研究所的芬顿表示,“这一机制首次解释了这些与临床神经和精神记忆障碍息息相关的实验结果。”
作者简介:
李诺林,临床医学专业,因对神经科学的兴趣转为从事神经科学研究。
参考文献:(上下滑动可浏览)
1. Crick F. Neurobiology: Memory and molecular turnover. Nature. 1984;312(5990):101-.2.
2. How do our memories last a lifetime? New study offers a biological explanation 2024 [Available on: https://www.sciencedaily.com/releases/2024/06/240626152118.htm.
3. Tsokas P, Hsieh C, Flores-Obando RE, Bernabo M, Tcherepanov A, Hernández AI, et al. KIBRA anchoring the action of PKMζ maintains the persistence of memory. Sci Adv. 2024;10(26):eadl0030.
4. Memories “Stick” Thanks to Two-Molecule Synaptic Tagging Mechanism [Available on:
- 新加坡国立大学仇成伟教授:意...
- 托马斯·弗里德曼:中美关系究...
- 2023美国USNEWS最佳...
- 哈佛读博 残疾中国姑娘逆袭人...
- 2023年CSC与有关国际组...
- 美国国家侦察局(NRO):计...
- 剑桥大学设计出低成本、高能效...
- 美国晨光基金会2023年奖助...
- 哥伦比亚大学与百人会联合发布...
- 2023年中国毒情形势报告...
- 2023WRWU世界大学排名...
- 为什么中国基础研究难获诺贝尔...
- 四个中立国家倒戈,转向军援乌...
- 美国安顾问沙利文在布鲁金斯学...
- 2023年全球最佳医院排行榜...
- 密歇根州立大学博士生身穿自己...
- 让HIV无法进入细胞 麻省总...
- 《天体物理学杂志快报》:全分...
- 美国西来大学陈岳云教授:40...
- 伦敦大学学院教授唐军旺院士实...
- 德国马克斯·普朗克太阳系研究...
- 谷歌科学家Natasha J...
- 中国教育部、海南省《境外高等...
- ChatGPT助力科研:智能...
- 洛杉磯西來大学欢迎您!...
- 2023年5月美国移民排期进...
- 2023年(第十五届)苏州国...
- 直接读取人类思维的机器来了!...
- 2024年度日本政府(文部科...
- 我在印度生活8个月,摘下有色...
Scholars-Net is a 501(c)(3) non-profit organization. Check payable to CAPPA, P.O. Box 236, Barstow, CA 92312, or direct deposit to Cathay Bank, 9121 Bolsa Ave., Westminster, CA 92683. Account number: 0005479070






